Categoría: medicamentos de uso humano
Referencia: MUH, 4/2021
- El CAR-T ARI-0001 es el primer CAR-T desarrollado en Europa autorizado para su uso en pacientes
- La AEMPS ha emitido una autorización de uso para medicamentos de terapia avanzada de fabricación no industrial, lo que permitirá tratar pacientes con leucemia linfoblástica aguda resistentes a tratamientos convencionales que hasta ahora no tenían más opciones terapéuticas
- En un ensayo clínico realizado en el Clínic y en el Hospital Sant Joan de Déu, el CAR-T ARI-0001 demostró ser seguro y eficaz
La Agencia Española del Medicamento y Productos Sanitarios (AEMPS) ha aprobado el uso como medicamentos de terapia avanzada de fabricación no industrial el CAR-T ARI-0001, desarrollado por el Hospital Clínic, para su utilización en pacientes mayores de 25 años con Leucemia Linfoblástica resistente a los tratamientos convencionales. Se trata del primer CAR-T desarrollado íntegramente en Europa que es aprobado por una agencia reguladora.
La autorización excepcional de uso por parte de la AEMPS supone un hito en nuestro país, pues es el primer tratamiento con células modificadas genéticamente que lo consigue. Esta autorización forma parte del Plan de abordaje de Terapias Avanzadas en el Sistema Nacional de Salud, del Ministerio de Sanidad.
Hoy lo han explicado en rueda de prensa el Dr. Josep M. Campistol, Director General del Clínic; el Dr. Álvaro Urbano-Ispizua, Director del Instituto Clínic de Enfermedades Hemato-Oncológicas; el Dr. Manel Juan, Jefe del Servicio de Inmunología al Centre de Diagnòstic Biomèdic (CDB) del Clínic y responsable de las plataformas conjuntas de Hospital Sant Joan de Déu i Banc de Sang i Teixits; el Dr. César Hernández, Jefe del Departamento de medicamentos de uso humano de la AEMPS y la Dra. Xènia Acebes, Directora del Área Asistencial del Servei Català de la Salut (CatSalut).
El Dr. Josep M. Campistol, comenta que “llegar hasta aquí ha sido posible gracias al esfuerzo conjunto de muchos profesionales e investigadores del hospital que han participado en las diversas etapas del desarrollo del tratamiento, desde la puesta a punto del CAR-T, hasta la realización del ensayo para demostrar su eficacia. Además, hemos contado con el impulso de la sociedad, a través del Proyecto ARI, para hacer realidad este proyecto que refleja la vocación del Clínic de ofrecer las alternativas de tratamiento más innovadoras a nuestros pacientes”.
El Dr. César Hernández apunta que “la autorización de uso que se concede en base a esta legislación de medicamentos de terapia avanzada de fabricación no industrial debe permitir, tanto el acceso de pacientes que no tienen otras alternativas de tratamiento, como continuar generando conocimiento sobre el medicamento para que, eventualmente, se consiga una autorización de comercialización centralizada para toda Europa”.
La Dra. Xènia Acebes señala que “con la exención de uso hospitalario del CAR-T ARI 001, queda patente que el Sistema de Salud de Cataluña está a la vanguardia de las terapias avanzadas. Los resultados se han conseguido gracias a la colaboración entre instituciones y la perseverancia de los equipos, que ha permitido desarrollar y autorizar esta terapia para una patología grave, con una indicación nicho. El Servicio Catalán de la Salud apuesta fuerte para desarrollar tratamientos innovadores. Sin duda, este es un punto de partida para el crecimiento de las terapias avanzadas en Cataluña y también para otras CAR que se puedan producir en nuestra casa”.
Un CAR-T desarrollado con una molécula propia
El CAR-T (Chimeric Antigen Recetor T-Cell) es un tipo de terapia celular y génica en la que el paciente se convierte en su propio donante. Consiste en modificar los linfocitos T del paciente para que tengan la capacidad de atacar a las células tumorales. “En nuestro caso, el CART lo hemos desarrollado a partir de un anticuerpo propio creado en el hospital hace más de 30 años”, explica el Dr. Manel Juan.
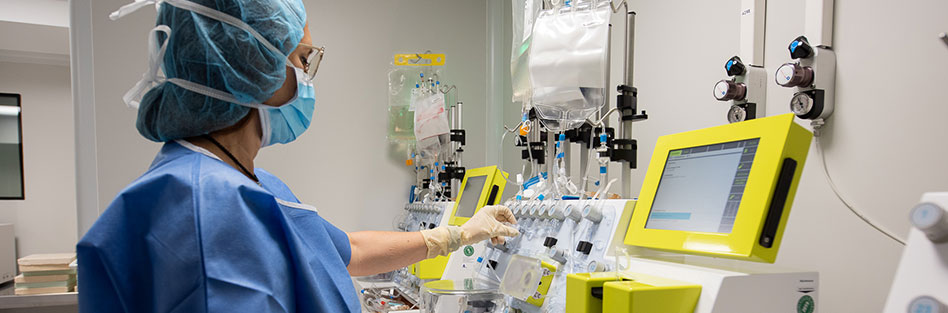
Mediante la aféresis, una técnica que permite la separación de los componentes de la sangre, se obtienen los linfocitos T, un tipo de glóbulos blancos encargados de la respuesta inmunitaria. Estos se reprograman genéticamente para que, cuando sean transfundidos de nuevo al paciente, puedan reconocer específicamente las células tumorales y atacarlas. Pasadas tres semanas ya se puede observar la respuesta en el paciente.
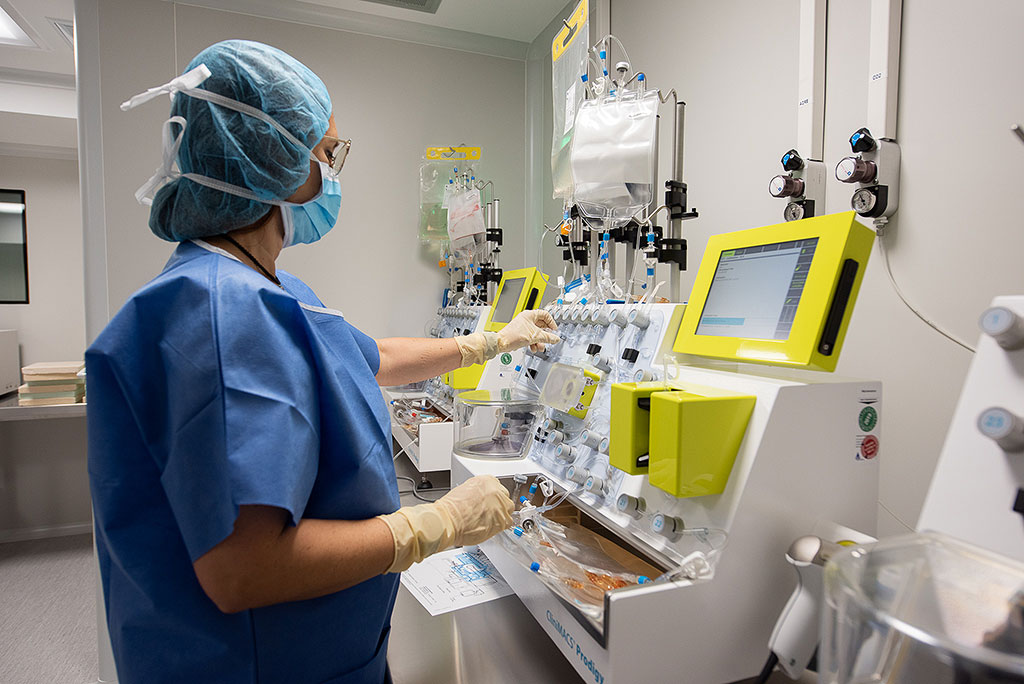
Fotografía: Francisco Avia
Con el objetivo de poner a disposición de los pacientes este tratamiento, un equipo liderado por el Dr. Manel Juan, desarrolló un nuevo CAR-T CD19 a partir del anticuerpo monoclonal propio para modificar los linfocitos T. Los estudios preclínicos demostraron que el CAR-T ARI-0001 era capaz de controlar por completo la progresión de la enfermedad en modelos animales y que su eficacia era similar a la de otros CAR-T disponibles. “El método de preparación utilizado para la obtención de nuestro CAR-T es robusto y reproducible y permite rebajar el coste de producción de la terapia para hacerla asequible a las instituciones académicas y que esté disponible para todos los pacientes”, apunta el Dr. Juan.
Un ensayo clínico para tratar a pacientes sin alternativas terapéuticas
La leucemia linfoblástica aguda (LLA) es uno de los cuatro tipos principales de leucemia y se caracteriza por una producción excesiva de linfocitos, o glóbulos blancos, inmaduros que se multiplican de forma rápida y desplazan a las células normales de la médula ósea. Aunque en la mayoría de los casos se consigue una remisión completa con quimioterapia o con el trasplante de médula ósea, entre un 10% y un 15% de los pacientes fallecen por resistencia al tratamiento, por su toxicidad o por una recaída. Cuando las opciones de tratamiento se agotan, hacen falta soluciones menos tóxicas y más dirigidas en las que la inmunoterapia puede jugar un papel fundamental.
El ensayo clínico se llevó a cabo en el Hospital Clínic y el Hospital Sant Joan de Déu de a partir de julio de 2017. Se incluyeron 58 pacientes adultos y pediátricos, de los cuales, 38 con LLA fueron tratados con el CAR-T desarrollado en el Clínic. Todos los pacientes habían recibido varias líneas de tratamiento y la gran mayoría habían sido trasplantados con médula ósea. Se trataba por tanto de pacientes sin alternativas terapéuticas disponibles.
Los resultados del ensayo demuestran que el CAR-T ARI-0001 produce una respuesta completa en más de una 70% de los pacientes, esto significa que no queda enfermedad residual. El Dr. Álvaro Urbano-Ispizua explica que “nuestro CAR-T es seguro y muy eficaz, con unos resultados comparables a los descritos para otras terapias CAR-T”.
“El hecho de producirlo en nuestro propio hospital hace que podamos prepararlo en muy poco tiempo, un aspecto fundamental teniendo en cuenta la fragilidad de muchos de estos pacientes. Además, podemos adecuar el tratamiento en función de las características del paciente. Además, al tener el producto en nuestras manos, podemos modular la cantidad de CARTs a administrar o repetir la dosis, si fuera necesario”, señala el Dr. Urbano-Ispizua.
El Dr. Gonzalo Calvo, Jefe de Servicio de Farmacología Clínica del Área del Medicamento del Hospital Clínic, ha liderado un grupo de profesionales que se han encargado de elaborar la solicitud de aprobación y mantener el diálogo necesario con la AEMPS para que se produjera esta autorización garantizando la calidad, seguridad y eficacia del tratamiento. El Dr. Calvo comenta que “la evaluación realizada por la AEMPS del CAR-T ARI-0001 se ha llevado a cabo siguiendo los estándares reguladores europeos y aplicado la legislación española para terapias avanzadas de fabricación no industrial, y garantiza que el CAR-T del Clínic es un medicamento que cumple los criterios de calidad, seguridad y eficacia exigibles en nuestro entorno”. Con esta autorización de uso se seguirá generando conocimiento sobre este CAR-T al tiempo que pacientes que no tienen otras alternativas se benefician de la posibilidad de acceder al mismo.
El Proyecto ARI, motor del CAR-T en el Clínic
El Proyecto ARI nació del sueño del Ari Benedé, una chica diagnosticada de LLA que nos dejó el 2 de septiembre de 2016. Ella y su madre, Àngela Jover, pusieron en marcha este Proyecto, basado en dos líneas de actuación: la investigación, centrada en la implantación en el Clínic de los CARs, y la asistencia, con el objetivo mejorar la atención domiciliaria de pacientes oncológicos y hematológicos. “Con el Proyecto ARI empezó todo. No sólo los recursos económicos necesarios, sino la motivación, la ilusión, el trabajo en equipo. Siempre estaremos en deuda con Ari”, afirma el Dr. Urbano-Ispizua.
El Proyecto ARI recaudó cerca de 1,8 millones de euros provenientes de empresas, fundaciones y asociaciones y particulares.