La evaluación de tecnologías sanitarias (ETS) permite a las autoridades decidir sobre la incorporación, financiación, precio, reembolso o desinversión de las mismas, con el objetivo de asegurar un sistema sanitario equitativo y eficiente.
La ETS puede mejorar la evidencia científica utilizada para la toma de decisiones clínicas y el acceso de los pacientes a las tecnologías sanitarias, incluso cuando una tecnología sanitaria se vuelve obsoleta.
El resultado de la ETS se utiliza para fundamentar las decisiones relativas a la asignación de recursos presupuestarios en el ámbito de la salud, por ejemplo, en relación con el establecimiento de los niveles de precios o de reembolso de las tecnologías sanitarias.
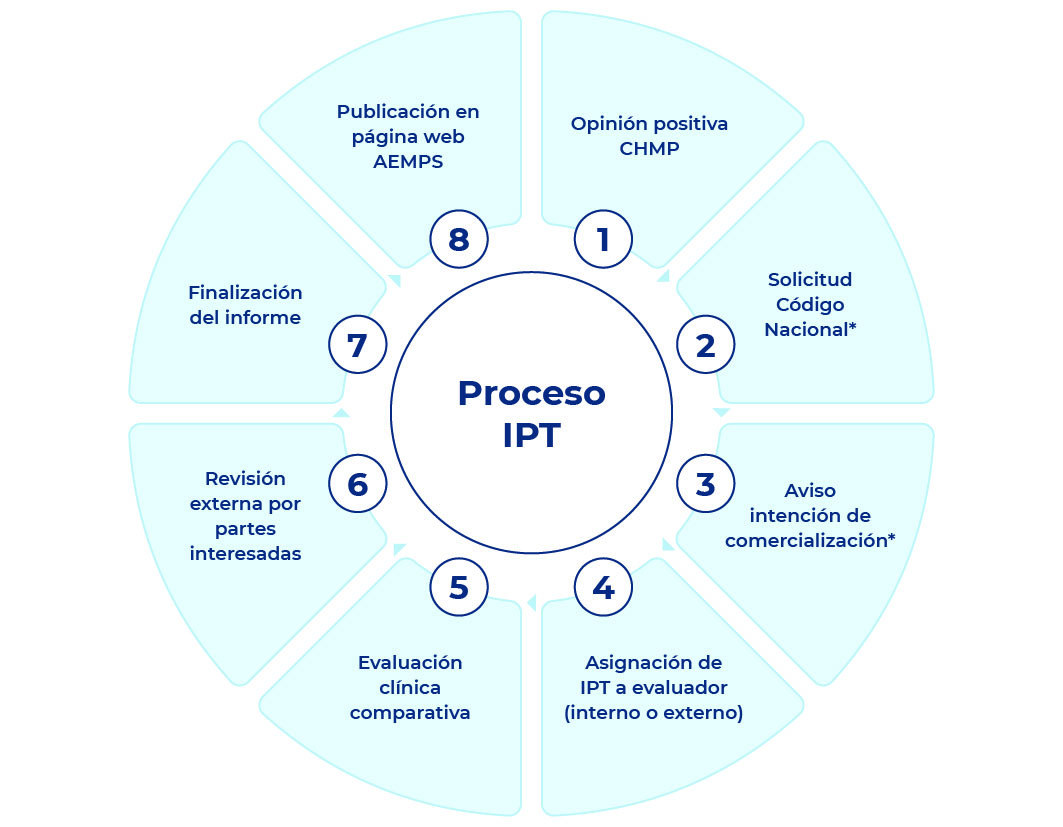
*Si se trata de una nueva indicación que corresponde a un medicamento con IPT previo y no implica una nueva presentación, estos dos pasos no son necesarios.
En España, la AEMPS y la Dirección General de Cartera Básica del Servicio Nacional de Salud y Farmacia (DGCBSF) deben evaluar los medicamentos de uso humano para su incorporación efectiva a la práctica asistencial. La Agencia realiza la ETS a través de los Informes de Posicionamiento Terapéutico. Los IPTs son reconocibles para todo el SNS a través de un sistema de evaluación en red basado en la evidencia científica.
Historia de la Evaluación de tecnologías sanitarias en la AEMPS
IPT
Desde 2013, La AEMPS y la DGCBSF realizan un único IPT reconocible por todo el SNS, con el mismo beneficio final para cada uno de ellos, manteniendo la coherencia en la evaluación y compartiendo los recursos de forma más eficiente.
AEMPS entra en EUnetHTA
La AEMPS empieza a participar en las acciones conjuntas previas de la red europea de evaluación de tecnologías sanitarias EUnetHTA desde 2016.
CE adopta la propuesta de reglamento de ETS
La Comisión Europea adoptó su propuesta de reglamento sobre evaluación de tecnologías sanitarias el 31 de enero de 2018.
Se establece el Grupo de Jefes de Agencias de ETS
Se establece el Grupo de Jefes de Agencias de ETS (HAG, Heads of HTA Agencies, por sus siglas en inglés) en septiembre de 2021. La AEMPS es miembro del HAG.
Adopción del Reglamento (UE) 2021/2282
El Reglamento (UE) 2021/2282 fue adoptado en diciembre de 2021, un resultado clave de la Estrategia Farmacéutica Europea.
Entrada en vigor del Reglamento (UE) 2021/2282
El Reglamento (UE) 2021/2282 entró en vigor en enero de 2022.
Preparación para la entrada en aplicación del reglamento
La AEMPS ha participado activamente en la preparación para la entrada en aplicación del reglamento desde 2022.
La AEMPS empieza a formar parte del Member State Coordination Group on HTA
En junio de 2022 la AEMPS empieza a formar parte del Member State Coordination Group on HTA (HTACG) de la Comisión Europea, que busca coordinar y adoptar el trabajo conjunto de ETS realizado por sus subgrupos en el ámbito de aplicación del presente Reglamento y adoptar documentos de orientación metodológica y procedimental para el trabajo conjunto.
AEMPS entra en los cuatro subgrupos (JCA, JSC, EHT, MPG)
En abril del 2023, la AEMPS empieza a formar parte de los cuatro subgrupos. Los subgrupos incluyen evaluaciones clínicas conjuntas (JCA, por sus siglas en inglés), consultas científicas conjuntas (JSC, por sus siglas en inglés), identificación de tecnologías sanitarias emergentes (EHT, por sus siglas en inglés) y desarrollo de orientaciones metodológicas y procedimentales (MPG, por sus siglas en inglés).
AEMPS asume la co-presidencia del subgrupo de Consultas Científicas Conjuntas
En febrero de 2024, la AEMPS asume la co-presidencia del subgrupo de Consultas Científicas Conjuntas.
La Comisión Europea adoptó, mediante actos de ejecución, normas de procedimiento detalladas
La Comisión Europea adoptó, mediante actos de ejecución, normas de procedimiento detalladas para medicamentos a lo largo de 2024. La Comisión Europea estuvo asistida por un comité, en el que estaban representados los Estados Miembros de la UE, entre los que estaban representantes de la AEMPS.
Entrada en aplicación del Reglamento (UE) 2021/2282
El Reglamento (UE) 2021/2282 sobre Evaluación de las Tecnologías Sanitarias (ETS), entró en aplicación el 12 de enero de 2025. Este reglamento crea un marco comunitario para la evaluación de tecnologías sanitarias que incluyen medicamentos y productos sanitarios y tiene por objetivo ayudar a las autoridades nacionales a tomar decisiones más informadas y oportunas sobre la fijación de precios y reembolso de las tecnologías sanitarias, así como agilizar el procedimiento para los desarrolladores de tecnologías sanitarias, contribuyendo a un acceso más rápido y amplio a productos innovadores y más eficaces para los pacientes.

