La AEMPS participa en el proyecto STARS, uno de los proyectos de la European Innovation Network (EU-IN, por sus siglas en inglés), financiado por la Comisión Europea. STARS tiene como objetivo mejorar el conocimiento regulatorio de los investigadores académicos, así como mejorar el impacto directo que este apoyo regulatorio tendrá en los resultados obtenidos por los mismos.
Se ha observado que, a menudo, existe una falta de conocimiento específico en ciencias regulatorias por parte de los investigadores de academia, lo cual retrasa el desarrollo de nuevas estrategias de tratamiento o limita la posibilidad de que innovaciones prometedoras lleguen a los pacientes.
De este modo, es crucial un intercambio de ideas en etapas tempranas del desarrollo y una buena comunicación entre investigadores de academia y reguladores.
El marco presentado en la Figura 1 resalta el flujo de información entre los distintos participantes del sistema regulatorio. A nivel nacional, las agencias reguladoras de cada país, que son las autoridades nacionales competentes (NCAs, por sus siglas en inglés), y la Agencia Europea de Medicamentos (EMA, por sus siglas en inglés), son clave tanto en la evaluación y autorización de medicamentos, como en la orientación sobre el diseño de su desarrollo con éxito. Para ello, utilizan canales específicos que llegan a los principales participantes de la academia, concretamente, a los investigadores clínicos de los centros médicos universitarios y hospitales. Otros partícipes incluyen a institutos, investigadores independientes trabajando en I+D y promotores públicos y privados, los cuales dan soporte económico a estas actividades de investigación. La Figura 1 ha sido desarrollada por el consortium STARS y publicada en el artículo “Strengthening regulatory science in academia: STARS, an EU initiative to bridge the translational gap” (Starokozhko et al., 2020).
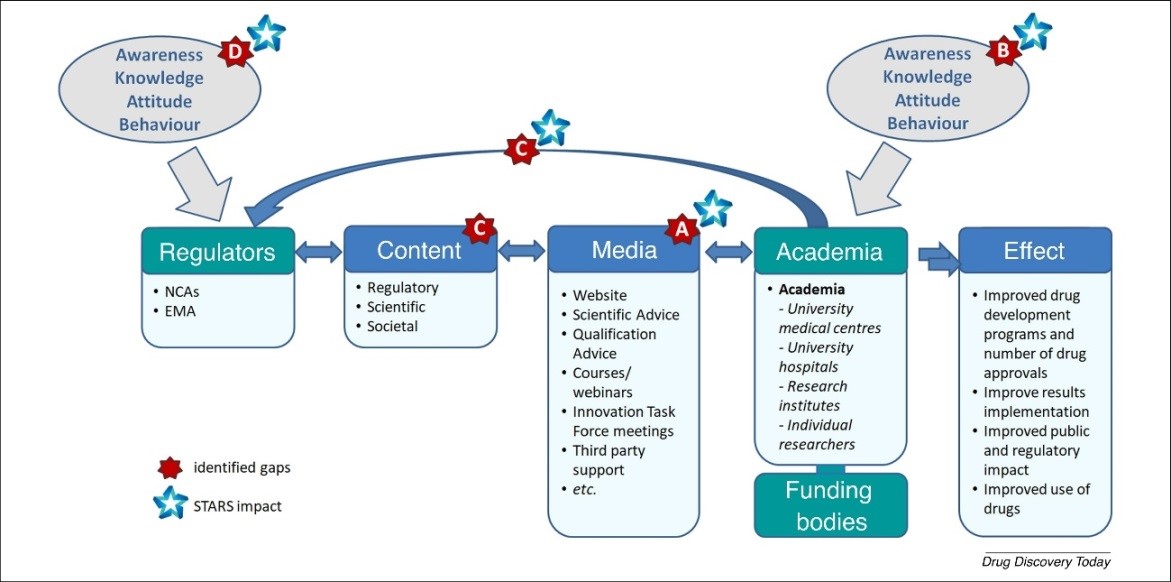
Figura 1. Flujo y gaps identificados en el marco de comunicación regulatorio (cf. STARS White Paper by Starokozhko et al., 2020).
STARS tiene el objetivo y el potencial de completar los gaps resaltados en la Figura 1 y coordinar y armonizar los esfuerzos regulatorios entre Estados miembros, con el fin de dar apoyo a los investigadores académicos en el campo de la salud para el beneficio de los pacientes.
El propósito es llegar a los investigadores académicos en las etapas más tempranas de la planificación de sus proyectos de investigación clínica, así como en la solicitud de financiación. Un segundo objetivo es reforzar el conocimiento regulatorio, en general, accediendo a los investigadores de academia durante su cualificación y capacitación profesional.
Se puede encontrar información adicional y las actividades actuales del proyecto en la página web de STARS
Se han realizado distintas actividades a través de los siguientes paquetes de trabajo o Work Packages (WP, por sus siglas en inglés):
- WP1: administración y coordinación del proyecto
- WP2: análisis de las actividades de apoyo existentes con el fin de elaborar un inventario. Tras la realización de este paquete de trabajo, STARS ha lanzado un inventario (Comprehensive Inventory) de actividades de apoyo para los investigadores de academia, con el fin de guiarlos en el enfoque regulatorio y científico necesario para el desarrollo de sus productos. Este inventario de actividades nace tras el análisis exhaustivo de los programas establecidos actualmente.
- WP3: análisis de las capacidades y de los servicios ofertados por parte de las NCAs y EMA.
-
WP4: realización de tres proyectos piloto
Piloto I: transferencia de un ejemplo de buenas prácticas de formación.
Piloto II: establecer una actividad nueva de apoyo regulatorio.
Piloto III: implementar un plan de formación curricular (Comprehensive Curriculum) para asegurar la elaboración de tutoriales armonizados que hagan referencia a contenido regulatorio y científico.
Finalmente, STARS emitirá recomendaciones consensuadas que aseguren el apoyo sostenible a los investigadores académicos y propondrá mecanismos adicionales de soporte, basados en un análisis profundo de las necesidades. Todas estas actividades alimentarán una estrategia común, que es el mapa de ruta para reforzar el conocimiento en ciencias regulatorias.
La AEMPS, a través de la Oficina de apoyo a la innovación y conocimiento sobre medicamentos, está liderando el Piloto II que se llevará a cabo durante el mes de septiembre exclusivamente en España.
Piloto II: OBJETIVO y PROCEDIMIENTO de STARS. Piloto II. Nueva actividad de apoyo
El Piloto II es uno de los tres pilotos del proyecto STARS y representa una nueva actividad de apoyo para reforzar el conocimiento regulatorio de los investigadores de academia.
El desarrollo de esta nueva actividad de apoyo se basa en los datos obtenidos de las diferentes encuestas llevadas a cabo a lo largo del proyecto STARS (WP2 y WP3).
Se preguntaron, a las distintas partes interesadas, aspectos sobre la concienciación, conocimiento y apoyo regulatorio. En total, se analizaron datos de 449 grupos de investigación académica en el campo de la salud, 88 centros de investigación en salud, 40 promotores y 21 autoridades nacionales competentes (NCAs), con el fin de identificar las buenas prácticas y gaps que poseen los participantes a nivel de concienciación, conocimiento y enfoque regulatorio en relación con la investigación académica.
Un análisis exhaustivo de los datos reveló, por un lado, que existe una necesidad por parte de la comunidad académica de herramientas que mejoren la comunicación entre reguladores y académicos y, por otro lado, que es necesaria una respuesta rápida y adecuada.
Basándose en estos hallazgos, el Piloto II se fundamenta en la creación de una Plataforma one-stop-shop donde los investigadores académicos van a poder encontrar contenido general sobre aspectos regulatorios, pero también van a poder enviar preguntas o cuestiones rápidas.
El objetivo de esta plataforma es facilitar el intercambio de información y orientación regulatoria durante el proceso de desarrollo por parte de los investigadores de academia, completando y reforzando los procedimientos regulatorios formales existentes (como la información y orientación obtenidas a través de las asesorías científicas nacionales, simultáneas o a través de las oficinas de innovación). Este servicio estará exento de tasas.
Para utilizar este servicio se podrá contactar con la AEMPS, cumplimentando la hoja de contacto (Contact sheet form), o mediante e-mail (stars_pilot2@aemps.es). Para más detalles, ver el apartado Communication Board.
Dentro de la Plataforma one-stop-shop, se encuentran las siguientes secciones:
- Explanation Board. Información general sobre el proyecto STARS y sobre el Piloto II.
- Information Board. Se incluirán múltiples documentos regulatorios y requisitos regulatorios y científicos para facilitar el desarrollo de medicamentos y, en un futuro, obtener la autorización de comercialización. De este modo, los investigadores podrán acceder a información regulatoria relevante ”en una sola parada”. La idea es que con esta información los investigadores sean capaces de resolver sus dudas y si no fuese así puedan contactar con la AEMPS (ver communication board).
- Communication Board. En esta sección los investigadores podrán encontrar información de contacto de la AEMPS (a través de la hoja de contacto o del e-mail (stars_pilot2@aemps.es).
- Feedback Board. El feedback de los investigadores es fundamental para evaluar el éxito del Piloto II. En el Feedback Board solicitaremos a los investigadores que participen en el piloto cumplimentar un pequeño cuestionario.
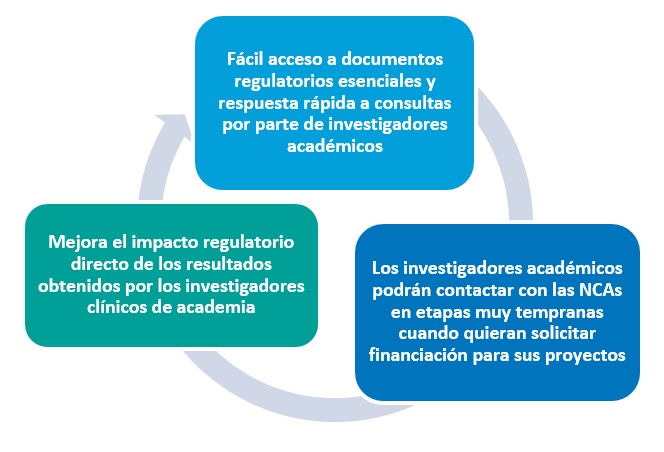
Figura 2. Concepto del Piloto II de STARS.
Invitación para participar en el piloto:
OBJETIVO y PROCEDIMIENTO del Piloto III de STARS
Implementación del plan de formación curricular
El Piloto III es uno de los tres pilotos del proyecto STARS financiado por la UE (Unión Europea), que representa la implementación de un plan de formación curricular para fortalecer el conocimiento regulatorio en el mundo académico. Está planificado y realizado por la AEMPS (Agencia Española de Medicamentos y Productos Sanitarios), en cooperación con el PEI (Instituto Paul Ehrlich, Alemania) y OGYEI (Instituto Nacional de Farmacia y Nutrición, Hungría), y cuenta con el apoyo de DLR/Agencia de Gestión de Proyectos (Centro Aeroespacial Alemán, Alemania).
El concepto del Piloto III
La rápida expansión de los productos farmacéuticos y biomédicos y la creciente complejidad de las tecnologías y productos innovadores tienden a comenzar en las instituciones de investigación no comerciales. Para cerrar la brecha traslacional, los profesionales altamente cualificados necesitan poseer conocimientos regulatorios para realizar investigaciones acordes a las complejas políticas regulatorias y procedimientos establecidos.
El plan de formación curricular de STARS (STARS Comprehensive Curriculum -CpC, por sus siglas en inglés) consta de cinco módulos: módulo del Core Curriculum y cuatro módulos más -módulo de calidad, módulo de preclínica, módulo de clínica y módulo de farmacovigilancia, tras la obtención de la autorización de comercialización-. Todos los módulos proporcionan información y conocimientos decisivos para desarrollar medicamentos, especialmente innovadores, junto con los requisitos regulatorios necesarios para lograr que los medicamentos que lleguen al mercado europeo posean la calidad, seguridad y eficacia adecuadas.
Teniendo en cuenta que el proyecto tiene una duración limitada, el Piloto III se centra en el STARS Core Curriculum, con algunas pinceladas de los temas incluidos en los otros módulos (ver Figura 1).
El formato del Piloto III se basará en una presentación denominada “Regulatory Support to Spanish Academia from STARS Core to Comprehensive Curriculum”, ya que la intención es que en un futuro se pueda ampliar incluyendo cada uno de los puntos que contiene cada uno de los módulos.
El contenido del Core Curriculum ofrece una visión general de los requisitos regulatorios, presentando los otros cuatro módulos, que se centran en cada una de las áreas mencionadas anteriormente, y relacionados con todo el ciclo de vida del medicamento.
Esta educación especializada es una herramienta clave para que los investigadores clínicos y científicos comprendan los requisitos regulatorios, se familiaricen con las directrices específicas que aplican a todo el ciclo de vida del medicamento, y para que conozcan el uso adecuado (en tiempo y forma) de las actividades de soporte de las NCA (Autoridades Nacionales Competentes, por sus siglas en inglés) durante el desarrollo de sus medicamentos (Figura 1).
El objetivo general es que los investigadores sean capaces de trasladar sus investigaciones al desarrollo clínico, con el fin de llegar cuanto antes a los pacientes.
Figura 1. Plan de formación curricular de STARS en ciencia regulatoria.
El Piloto III se ofrece de forma gratuita. Cuando los asistentes participen aceptarán responder a una breve encuesta para poder evaluar el Piloto III.
En caso de cualquier consulta sobre el Piloto no dude en ponerse en contacto con nosotros: stars_pilot3@aemps.es.
El Piloto se pone en marcha del 16 de febrero al 16 de marzo de 2022.
Pincha Aquí:
https://www.csa-stars.eu/Pilot-III-Implementing-the-Comprehensive-Curriculum-1761.html
¡Esperamos vuestra participación!
Oficina de apoyo a la innovación y conocimiento sobre medicamentos
e-mail: innov_spain@aemps.es
Para participar en el piloto III: stars_pilot3@aemps.es


