Categoría: productos sanitarios/seguridad
Referencia: PS, 20/2024
- El fallo no afecta a la administración de terapia pero una interrupción de ésta podría pasar desapercibida y causar una desaturación de oxígeno en el paciente.
- Los dispositivos Airvo 2 (uso hospitalario) y myAirvo 2 (uso domiciliario) no están diseñados para ser utilizados en soporte vital.
- La empresa fabricante está comunicando la retirada del mercado de determinados números de serie de estos equipos.
- La AEMPS establece una serie de recomendaciones dirigidas a los profesionales de la sanidad, proveedores de servicio de terapia respiratoria domiciliaria y pacientes.
La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS), ha tenido conocimiento a través del fabricante Fisher & Paykel Healthcare Ltd., Australia, de la retirada del mercado de determinados números de serie de respiradores de terapia respiratoria de alto flujo Airvo 2 y myAirvo 2, debido a que por problema en la configuración del altavoz podrían emitir alarmas sonoras de forma distorsionada, intermitente o inaudible.
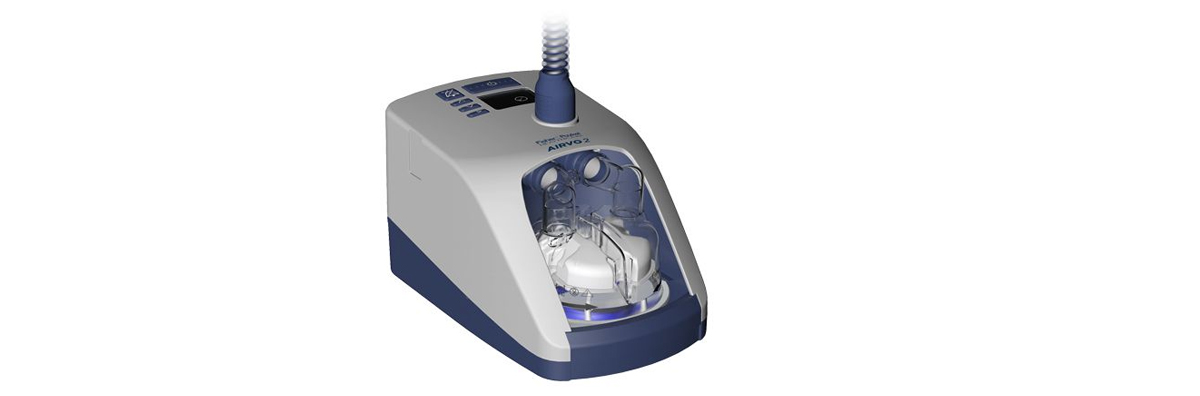
Airvo 2 y myAirvo 2 están destinados a administrar terapia respiratoria de alto flujo a los pacientes. Ninguno de los dos dispositivos están diseñados para ser utilizados en soporte vital.
De acuerdo con la información facilitada por la empresa, el altavoz de los dispositivos Airvo 2 y myAirvo 2 se ha diseñado para emitir alertas y alarmas sonoras al usuario en ciertas condiciones. En ausencia de una alarma sonora, si se produjera una interrupción de la terapia, ésta podría pasar desapercibida y causar una desaturación de oxígeno en el paciente.
Los dispositivos afectados fueron fabricados antes del 14 de agosto de 2017. En ellos la configuración del altavoz podría provocar que las alarmas sonoras se emitieran de manera distorsionada, intermitente o inaudible. Este problema no afectara a la administración de terapia por parte de los dispositivos Airvo 2 y myAirvo 2, ni a la alarma visual de la pantalla.
En los dispositivos fabricados con posterioridad al 14 de agosto de 2017, la empresa adoptó una nueva configuración de altavoz de un nuevo proveedor en la fabricación de los dispositivos Airvo 2 y myAirvo 2, por lo que los dispositivos fabricados después de esa fecha no están sujetos a esta retirada.
Situación actual en España
La empresa, Fisher & Paykel Healthcare, está enviando una nota de aviso a los distribuidores del producto, a las empresas de servicios de terapia respiratoria domiciliaria y a los profesionales de la salud que disponen de alguno de los equipos incluidos en el apartado “Productos afectados”, para informarles de este riesgo y de la retirada de las unidades afectadas en territorio español.
Productos afectados
| Nombre del dispositivo | Modelo | Intervalo nº de serie |
|---|---|---|
| Airvo 2* | myAirvo 2** | 120521YYYYYY – 170813YYYYYY |
| PT101XX | PT100XX |

*El producto Airvo 2 únicamente se distribuye a centros sanitarios.
** El producto my Airvo 2 se distribuye a través de empresas proveedoras de servicio de terapia respiratoria domiciliaria para ser utilizado por los pacientes en sus domicilios.

Fig 1: ejemplo de etiqueta de Airvo 2

Fig 2: ejemplo de etiqueta de myAirvo 2
Información para distribuidores
- Identifique los posibles equipos Airvo 2 y myAirvo 2 afectados en su inventario mediante la comprobación de la referencia y número de serie en la etiqueta del producto situada bajo la base de la unidad o en la etiqueta de la caja y ponga el equipo en cuarentena.
- Si ha distribuido el producto afectado a un centro sanitario, contacte con el centro para la retirada del producto y sustitución por un equipo no afectado.
Información para profesionales de la sanidad
- Si usted tiene un equipo Airvo 2 afectado en su centro, identifique si debe ser sustituido mediante la comprobación de la referencia y el número de serie en la etiqueta del producto, situada bajo la base de la unidad.
- En el caso de que el modelo/referencia de la etiqueta y el número de serie de su equipo coincidan con el modelo y números de serie incluidos esta nota de aviso, contacte inmediatamente con la empresa de servicios de terapia respiratoria domiciliaria/distribuidor que le ha suministrado el equipo para que se lo retiren y sustituyan por un equipo no afectado.
Información para proveedores de servicio de terapia respiratoria domiciliaria
- Identifique los posibles equipos myAirvo 2 afectados en su inventario mediante la comprobación de la referencia y número de serie en la etiqueta del producto situada bajo la base de la unidad o en la etiqueta de la caja y ponga el equipo en cuarentena.
- Identifique a los pacientes a los que haya distribuido el equipo, póngase en contacto con ellos para informarles de esta acción correctiva y sustituya los equipos afectados.
Información para pacientes/cuidadores
- Si usted tiene un equipo myAirvo 2 en su domicilio, identifique si debe ser sustituido mediante la comprobación de la referencia y número de serie en la etiqueta del producto, situada bajo la base de la unidad.
- En el caso de que el modelo/referencia de la etiqueta y el número de serie de su equipo coincidan con el modelo y números de serie incluidos esta nota de aviso, contacte inmediatamente con la empresa de servicios de terapia respiratoria domiciliaria que le ha suministrado el equipo para que se lo retiren y sustituyan por un equipo no afectado.
Datos de contacto de las empresas proveedoras de servicio de terapia respiratoria domiciliaria:
Estas empresas distribuyen únicamente myAirvo 2 a pacientes en sus domicilios:
- Vivisol Iberica, S.L.U., Calle del yeso, 2, 28500 Arganda Del Rey, Madrid.
- Palex Medical S.A, C/Jesús Serra Santamans, 5, 08174 Sant Cugat del Vallès, Barcelona
- Air Liquide Healthcare España S.L., Calle Orense, 34, 28020, Madrid.
- Oxigen Salud, S.A., Ctra. Rubí 141-143, 08174, Sant Cugat del Valles, Barcelona.
- Oximesa / NIppon Gases SLU, C/. de Orense, 11, 5ª Planta, Tetuán, 28020 Madrid.
- Esteve Teijin SL., Pasaje Ferrocarril 369 08860, Castelldefels (Barcelona).
- Linde Medica SLU., Camino Liria s/n, apartado correos 25, 46530 Valencia.
Datos de contacto de los distribuidores a centros sanitarios:
Estos distribuidores distribuyen únicamente Airvo 2 a centros sanitarios:
- Endook Europa SL. Calle Comercio 16 nave 6, Parque empresarial Servia 41960, Ginés, Sevilla.
- Consumar SL. Calle Albert Einstein 12, local 2, 38204 La Laguna-Santa Cruz de Tenerife, Canarias.
- Nestle España SA. Avda Países Catalanes 21-25, Esplugues de Llobregat, 08950 Barcelona.
- Dextromédica SL Avda Pío XII 1, 46009 Valencia.
- Suministros Sanitarios de Extremadura. Calle 13, nº 28, Pol. Ind. El Nevero, 06006 Badajoz.
- Suministros Galeno SL., c/ Zaire 10, Perillo 15172, A Coruña.
- Helianthus Medical SL. C/ Telecomunicaciones 25. Pol Ind. Urtinsa II, 28923 Alcorcón, Madrid.
- Marcon Médica SL., C/ Castillo Moratalla 3, Lorqui 30564 Murcia.
Si tiene conocimiento de algún incidente relacionado con el uso de un producto sanitario, notifíquelo a través del portal NotificaPS. Su colaboración notificando es esencial para tener un mayor conocimiento de estos productos y velar por su seguridad.