NIPO: 134-23-019-7
Información dirigida a profesionales sanitarios
ÍNDICE
- Introducción
- Notificaciones individuales de sospechas de acontecimientos adversos (AA)
- Modificaciones de ficha técnica y estudios posteriores a la autorización
- Procedimientos centralizados, descentralizados y de reconocimiento mutuo
- Comité de Seguridad de Medicamentos Veterinarios (CSMV)
- Comité Técnico del Sistema Español de Farmacovigilancia de Medicamentos Veterinarios (CTSEF-VET)
- Alertas e informaciones de seguridad no urgente (NUIS) por razones de farmacovigilancia
- Alertas por defectos de calidad
- Promoción de la farmacovigilancia veterinaria
- Participación en reuniones internacionales
Introducción
Pese a la extensa información aportada para garantizar la calidad, seguridad y eficacia durante la solicitud de autorización de comercialización, solo es posible contar con un conocimiento completo del comportamiento de los medicamentos veterinarios (MV) una vez que se han registrado. Es en estas condiciones reales de uso de los medicamentos veterinarios cuando pueden aparecer problemas de eficacia o de seguridad novedosos que pueden ser relevantes: por ejemplo, al administrarlo a especies animales no autorizadas (en base a los preceptos legales de prescripción excepcional); cuando se utiliza en las diferentes razas de cada especie, en diversas condiciones de manejo, o cuando se administra a animales con patologías concomitantes o que reciben tratamientos con más de un medicamento (circunstancia bastante común en el ámbito veterinario). Por otra parte, una vez registrado el MV, su uso normalmente alcanza a miles de animales y solo entonces pueden dar la cara acontecimientos adversos (AA) que tengan una incidencia muy baja y que no se han observado en los estudios preclínicos y clínicos.
Es aquí donde cobra importancia la actividad de Salud Pública que tiene por objeto la identificación, cuantificación, evaluación y prevención de los riesgos del uso de los MV una vez comercializados, permitiendo así el seguimiento de los posibles acontecimientos adversos, o lo que es lo mismo, farmacovigilancia (FV). Es por ello que se creó el Sistema Español de Farmacovigilancia de Medicamentos Veterinarios (mediante el Real Decreto 1246/2008), buscando confirmar si el balance beneficio/riesgo (B/R) del uso de los MV se mantiene dentro de los márgenes conocidos desde su autorización, identificando si hay nuevos riesgos o si la gravedad y/o frecuencia de los riesgos ya conocidos ha variado significativamente. En base a ello, se instauran medidas para evitar o minimizar sus consecuencias y poder así gestionar adecuadamente los riesgos para la salud pública, la sanidad animal y el medio ambiente.
Para el funcionamiento de este sistema es imprescindible la participación activa de los profesionales sanitarios, muy especialmente los veterinarios, dado que se nutre de las notificaciones realizadas por los mismos.
Es importante recordar que el hecho de que se observen acontecimientos adversos a un medicamento veterinario no debe ser considerado como algo extraordinario, ya que no hay ningún MV que sea totalmente inocuo o esté exento de poder causar reacciones, ni ningún MV que sea 100% eficaz. De ahí la necesidad de implementar un sistema de FV y una evaluación técnica del balance B/R, para aportar a todos los interesados (profesionales sanitarios, ganaderos, propietarios de los animales y usuarios en general) la mejor información que ayude a tomar las mejores decisiones de tratamiento en cada momento.
Conforme establece la legislación europea (Reglamento (UE) 2019/6), la FV cubre toda una serie de situaciones (más amplias que las que se contemplan en la FV de medicamentos de uso humano), incluyendo aspectos de seguridad y eficacia en los animales de destino; de seguridad en las personas que manipulan los MV o que entran en contacto con los animales a los que se les ha administrado el MV; en los consumidores de alimentos de origen animal (los problemas derivados de unos residuos mayores que los límites máximos de residuos –LMR– aprobados en la UE) con las consiguientes repercusiones en la salud pública, así como problemas medioambientales. De forma global, pueden considerarse como sospechas de AA los siguientes casos:
- Sospechas de reacciones adversas (RA) en animales en condiciones normales de empleo del MV, es decir, cuando su empleo es conforme con su autorización de comercialización y, por tanto, en línea con lo establecido en la ficha técnica o resumen de características del medicamento.
- RA tras el “uso no contemplado”, siendo éste el que corresponde a cualquier variación respecto a lo establecido en la autorización del MV.
- Sospecha de falta de la eficacia esperada.
- Insuficiencia de los tiempos de espera. La responsabilidad de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) es garantizar que si se respeta el tiempo de espera fijado en la autorización no aparecerán residuos por encima de los LMR en los alimentos de origen animal obtenidos de los animales tratados. De no ser así, se podría solicitar al titular la correspondiente variación para aumentar el tiempo de espera.
- Reacciones en personas, que se pueden producir durante la administración del producto a los animales, contacto con el mismo, inyecciones accidentales, etc.
- Problemas medioambientales, consecuencia de los tratamientos administrados a los animales.
- Transmisión de agentes infecciosos consecuencia de tratamientos con MV.
- Sospechas de reacciones adversas en animales a medicamentos de uso humano.
Las principales actividades que se llevan a cabo en el Departamento de Medicamentos Veterinarios (DMV) de la AEMPS son la gestión y evaluación de las notificaciones individuales de AA, ya sean comunicadas por profesionales sanitarios, propietarios de animales o ganaderos (bien directamente a través de la Tarjeta Verde o bien a través de la aplicación NotificaVET), o comunicadas por los titulares directamente a la base de datos de farmacovigilancia europea EVVET/UPhD. Desde el Área de Farmacovigilancia, Defectos de Calidad y Comercio Exterior de medicamentos veterinarios se realiza, asimismo, un seguimiento continuado de la calidad de los datos en EVVET/UPhD de los casos reportados en nuestro país, lo cual influye directamente en la ejecución de una detección de señales de calidad.
Además, se chequea un tipo de información que los titulares aportan dentro de cada procedimiento de registro, que son los resúmenes de los archivos maestros de los sistemas de farmacovigilancia (PSMF/AMSF), en los que describen cómo llevan a cabo las tareas principales de FV. Como consecuencia de toda esta labor, el Área de Farmacovigilancia Veterinaria de la AEMPS es responsable de proponer la instauración de medidas reguladoras, como son: obligar a los titulares a presentar variaciones de seguridad, la solicitud de estudios posautorización o, incluso, si el desequilibrio en el balance B/R no se pudiera corregir de manera efectiva, proponer la suspensión o la revocación definitiva de la autorización, decretando en estos supuestos una alerta.
Asimismo, el área evalúa y gestiona las alertas de FV y las notificaciones europeas no urgentes (NUIS) a nivel nacional e internacional, que son publicadas posteriormente en la web de la AEMPS, y el seguimiento y control de las medidas reguladores instauradas sobre las autorizaciones de los MV afectados en las alertas.
Por último, también se llevan a cabo, de forma periódica, los análisis de detección de señales de los MV autorizados por procedimiento centralizado de los que somos ponentes, así como de los MV autorizados por procedimiento de reconocimiento mutuo o descentralizado y nacional, siempre que sea necesario. Este trabajo está coordinado a nivel europeo por el P-SMEG (Pilot Signal Management Expert Group), del que forma parte la AEMPS. Para ello, se utiliza el repositorio unificado (Data Warehouse) que permite realizar búsquedas en EVVET/UPhD, donde se accede a todos los acontecimientos adversos que se hayan notificado, tanto en la UE como en países terceros. De esta forma, a pesar de que, de acuerdo a la nueva legislación, los titulares tienen la responsabilidad de supervisar la farmacovigilancia de sus productos, desde el Área de Farmacovigilancia, del Departamento de Medicamentos Veterinarios de la AEMPS, se realiza un seguimiento continuado de la misma, con el fin de detectar y/o complementar los datos que pudieran revelar un cambio en el B/R. El presente boletín recoge las actividades de FV llevadas a cabo por la AEMPS a través del Departamento de Medicamentos Veterinarios, siendo una herramienta básica de comunicación entre todos los implicados en general y, especialmente para los profesionales de la veterinaria, sobre la vigilancia continua de la eficacia y seguridad de los MV.
Notificaciones individuales de sospechas de acontecimientos adversos (AA)
La notificación o comunicación de un AA a un medicamento veterinario es obligatoria conforme la legislación nacional tanto para los profesionales sanitarios como para los titulares. Para armonizar y simplificar estas notificaciones en la UE, la red de agencias europeas de medicamentos veterinarios elaboró un formulario para uso exclusivo por profesionales sanitarios, que en España se ha editado en formato papel, conocido como Tarjeta Verde. Actualmente, la AEMPS también posee otro sistema de notificación electrónica: NotificaVET, de reciente creación, dirigido a profesionales sanitarios y al público en general.
NotificaVET tiene también la opción para que el público en general notifique sospechas de AA con otro formulario más adaptado. Independientemente de la vía de notificación (Tarjeta Verde, NotificaVET, etc.) toda esta información se incorpora a la base de datos nacional de FV (VIGÍA-VET-2), y una vez validada dicha información, se registra en la base de datos europea EVVET/UPhD.
Además, la aplicación de prescripción veterinaria del Consejo General de Colegios Veterinarios (PRESCRIVET), así como la del Consejo General de Colegios Veterinarios de Andalucía (RECEVET), cuentan con un espacio de notificación de sospechas de acontecimientos adversos. El número de notificaciones de AA en España en 2022 alcanzó las 4.208.
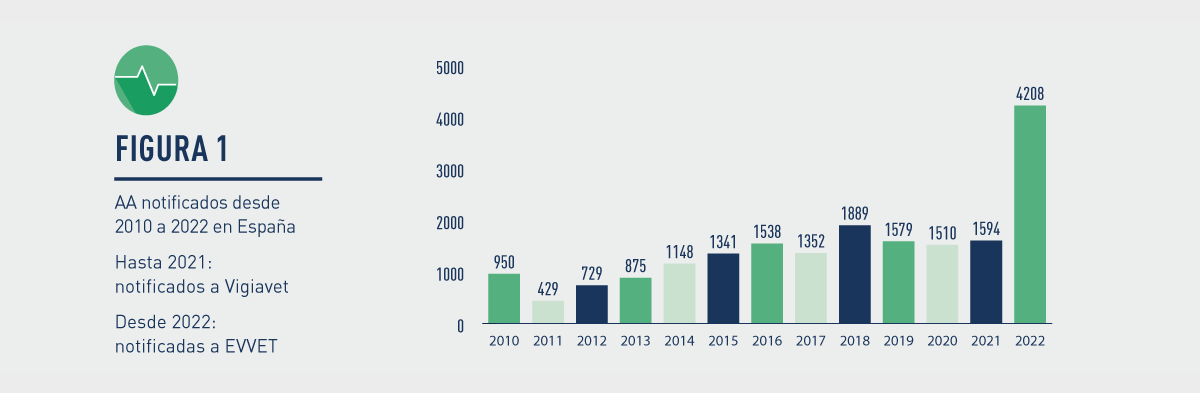
Gráfico 1 – AA notificados desde 2010 a 2022 en España
La diferencia de casos entre 2021 y 2022 se debe al cambio de legislación, tras el cual los titulares tienen que notificar individualmente a EVVET todos los casos -graves y no graves-. Antes del 28 de enero de 2022 solo tenían obligación de notificar aquellas sospechas de acontecimientos adversos clasificadas en la anterior legislación como “expeditivas”, permitiéndose que las “no expeditivas” se acumulasen en los line listing de los Informes Periódicos de Seguridad, donde no se podían realizar consultas y conocer exactamente los casos ocurridos en cada Estado. La base legal vigente con respecto a la obligatoriedad de comunicación y registro de las sospechas recibidas por los titulares, se refleja en el artículo 76 del Reglamento 2019/6.

Gráfico 2 – Distribución de las AA iniciales por especie animal afectada (sólo en aquellas en las que se han notificado más de cinco casos) en 2022
En cuanto a la estratificación de estos AA en 2022, las especies de destino en las que se presentaron fueron las siguientes: perro, gato, bovino, ovino, cerdo, conejo, aves de corral, caballo, caprino, hurón y abejas.
Menos de cinco casos ocurrieron en las siguientes especies: burros, peces (lubinas) y otras aves (loros, periquitos).
Además, 30 casos afectaron a personas.
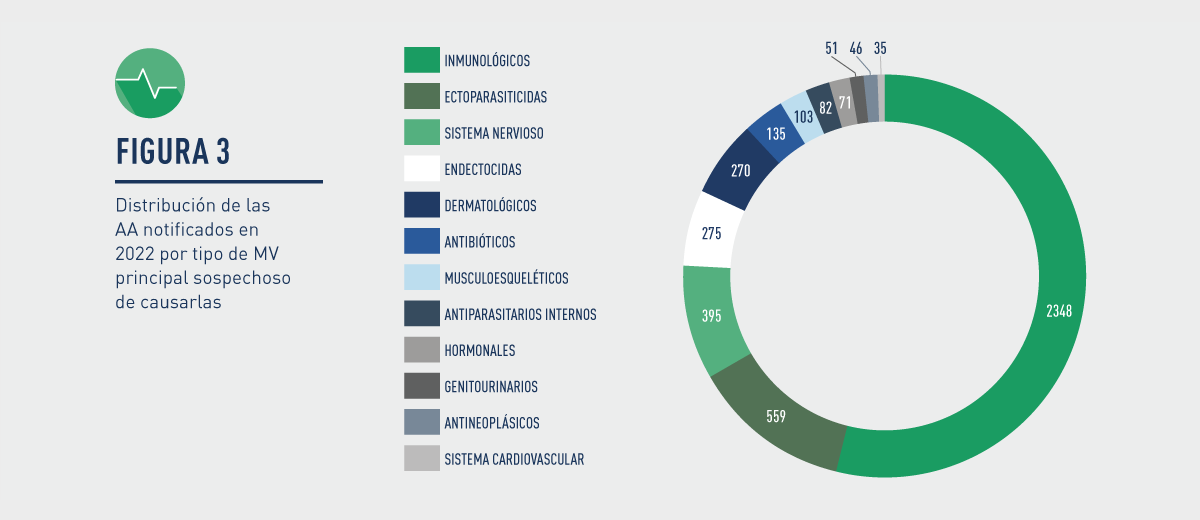
Gráfico 3 – Distribución de las AA notificadas en 2022 por tipo de MV principal sospechoso de causarlas
Con respecto a los medicamentos veterinarios implicados, los grupos en los que más frecuentemente se ha notificado corresponden a vacunas, ectoparasiticidas, agentes neurológicos, endectocidas, dermatológicos y antimicrobianos.
Tras ellos, se encuentran los medicamentos del sistema musculoesquéletico, antiparasitarios internos, hormonales, sistema genitourinario, antineoplásicos, sistema cardiovascular y sistema digestivo.
Otros medicamentos implicados con menos de 35 casos: sistema digestivo (31), órganos sensoriales (ojo, oído) (31), sistema respiratorio (8) y sangre (3).
Respecto del origen de las notificaciones iniciales de casos ocurridos en España, en 2022 de nuevo fue mayoritaria la realizada por los titulares (4.002 AA, un 95.1% del total), frente al resto de posibles orígenes (profesionales sanitarios, ganaderos, propietarios de animales, otros usuarios, etc.), que notificaron 206 AA, el 4.89%.
Conforme se establece en la normativa europea, la AEMPS ha enviado todas las AA notificadas en España a EVVET, en un plazo máximo de 30 días.

Gráfico 4 – Origen de las AA notificadas a la AEMPS en 2022
Modificaciones de ficha técnica y estudios posteriores a la autorización (EPA)
La legislación europea establece una serie de obligaciones en materia de FV para los titulares y entre ellas cabe destacar la de la realización de una detección de señales para cada uno de sus medicamentos, al menos una vez al año. Tras ello, si se observara un cambio en la relación beneficio/riesgo en alguno de sus medicamentos, la legislación establece la remisión por parte de los titulares de una variación para modificar las condiciones de autorización del medicamento. En el año 2022, se recibieron 85 variaciones, bien para adaptación de los textos a la nueva legislación (37 medicamentos) o cambios en los mismos por motivos de seguridad (48 medicamentos).
Tras su evaluación y, en su caso, previo dictamen del Comité de Seguridad de Medicamentos Veterinarios (CSMV), en nueve medicamentos se concluyó que era necesario proceder a la modificación de las fichas técnicas.
Por otro lado, con respecto a los ensayos posteriores a la comercialización, se recibieron seis notificaciones y una de autorización para este tipo de procedimientos, todos relacionados con problemas de farmacovigilancia y con el objeto de aclarar la causa de los mismos.
Procedimientos centralizados, descentralizados y de reconocimiento mutuo
En relación con el procedimiento de vigilancia y detección de señales de MV centralizados en EVVET/UPhD, en el año 2022 se realizaron 18 análisis, correspondientes a las revisiones para la detección de señales de los medicamentos de los que España es ponente: BTVPUR, Prac-tic, Spironolactone CEVA, Kexxtone, Meloxidolor, UpCard, Cardalis, Letifend, Sedadex, Eravac, Cepedex, Halagon, Clevor, Forceris, Isemid, Neptra, Tulissin y Syvazul BTV. Asimismo, y en el marco del P-SMEG (Pilot Signal Management Expert Group, grupo de trabajo de farmacovigilancia de la EMA) se realizaron otras cuatro detecciones de señales (Halocur, Kriptazen, Zulvac 1+8 ovis y Zulvac 8 ovis) de las que España es responsable.
Además de ello, se ha realizado por este procedimiento un Signal Detection “ad hoc” en diferentes grupos de medicamentos, y un Targeted Signal Management sobre un grupo de medicamentos, cuyo estudio lidera España como responsable.
Comité de Seguridad de Medicamentos Veterinarios (CSMV)
El CSMV es el órgano colegiado de la AEMPS creado para el asesoramiento técnico y científico en todo lo relativo a farmacovigilancia de los MV.
En 2022 se celebraron dos reuniones, en las que se trató la modificación de la autorización de comercialización de un total de 85 MV. Como en el resto de comités de la AEMPS, se publicaron en la web de la Agencia las correspondientes notas informativas de las reuniones celebradas. La última de estas reuniones se realizó conjuntamente con el Comité Técnico del Sistema Español de Farmacovigilancia Veterinaria (SEF-VET).
Los dictámenes del CSMV y los cambios acordados en procedimientos de reconocimiento mutuo, descentralizado y de renovaciones de autorizaciones de comercialización que fueron sometidos a evaluación o información del CSMV, junto a los que se presentaron para información, fueron los siguientes:
| MEDICAMENTO | PROPUESTA DE MODIFICACIÓN DE LOS TEXTOS |
|---|---|
| EQVALAN DUO (1596 ESP) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluyen signos digestivos, así como una frase en relación a la información al veterinario de otros efectos adversos. |
| STRONGHOLD PLUS 15 mg/2,5 mg SOLUCIÓN PARA UNCIÓN DORSAL PUNTUAL PARA GATOS HASTA 2,5 KG STRONGHOLD PLUS 30 mg/5 mg SOLUCIÓN PARA UNCIÓN DORSAL PUNTUAL PARA GATOS DE MÁS DE 2,5 HASTA 5 kg STRONGHOLD PLUS 60 mg/10 mg SOLUCIÓN PARA UNCIÓN DORSAL PUNTAL PARA GATOS DE MÁS DE 5 HASTA 10 kg (EU/2/16/204/005-003-001) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluyen síntomas neurológicos y digestivos. |
| ASTHENODEX 0,5 mg/ml SOLUCIÓN INYECTABLE PARA PERROS Y GATOS (3453 ESP) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se elimina información al respecto y se incluye tabla de frecuencias. |
| DEXMOPET 0.5 mg/ml SOLUCIÓN INYECTABLE PARA PERROS Y GATOS (3453 ESP) |
En el apartado 4.5 de Ficha Técnica y 12 del Prospecto, se elimina información al respecto y se incluye tabla de frecuencias en el 4.6 FT y 6 del prospecto. |
| GALLIFEN 40 mg/g PREMEZCLA MEDICAMENTOSA PARA POLLOS Y FAISANES (3414 ESP) |
En el apartado 4.5 de Ficha Técnica y 12. del Prospecto, se incluye información relativa a efectos tóxicos en mujeres embarazadas, toxicidad vía oral y efectos en piel. |
| BUPREDINE MULTIDOSIS 0,3 mg/ml SOLUCIÓN INYECTABLE PARA PERROS, GATOS Y CABALLOS (3374 ESP) |
Se modifica y/o actualiza información en el apartado 4.5 y 4.7 del SPC, sobre toxicidad tras el contacto con el producto y sobre teratogenicidad (ratas). |
| TUDOMAX 10 mg/g POLVO PARA ADMINISTRACIÓN EN AGUA DE BEBIDA O EN LECHE (3517 ESP) |
En el apartado 4.5 del SPC y 12 del prospecto, así como en el apartado 4.8, se incluye información sobre síntomas digestivos y respiratorios en personas y sobre interacciones con antibióticos. |
| VIRBACTAN 150 mg POMADA INTRAMAMARIA (1612 ESP) |
En el apartado 4.6 del SPC y 6. Del prospecto, se incluye información sobre reacciones de hipersensibilidad. |
| LETIFEND LIOFILIZADO Y DISOLVENTE PARA SOLUCIÓN INYECTABLE PARA PERROS (EU/2/16/195/001) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto se incluye información sobre reacciones de hipersensibilidad y anafilaxia. |
| BOLFO COLLAR (216 ESP) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluye información sobre reacciones locales y síntomas digestivos. |
| GLEPTOFERRON LABIANA 200 mg/ml SOLUCIÓN INYECTABLE (3575 ESP) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se actualiza el texto sobre reacciones locales y muerte en lechones. |
| CANIGEN L SUSPENSIÓN INYECTABLE PARA PERROS (3545 ESP) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluye información sobre reacciones locales y síntomas digestivos, de hipersensibilidad y anafilaxias. |
| CANIGEN PI/L (3546 ESP) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluye información sobre reacciones locales y síntomas digestivos, de hipersensibilidad y anafilaxias. |
| FLOXYME 50 mg/ml SOLUCIÓN PARA ADMINISTRACIÓN EN AGUA DE BEBIDA (2831 ESP) |
En el apartado 4.5 de Ficha Técnica, y 12 del prospecto, se incluye la frase siguiente: “No usar el medicamento con agua clorada”. |
| VECTRA FELIS SOLUCIÓN SPOT-ON PARA GATOS (EU/2/14/165/001) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluye información sobre signos neurológicos, y en el apartado 4.5, información sobre efectos tras la ingestión accidental. |
| FLOROLAB 100 mg/ml SOLUCIÓN PARA ADMINISTRACIÓN EN AGUA DE BEBIDA PARA PORCINO (3816 ESP) |
En el apartado 4.9 de Ficha Técnica se añade la frase siguiente: “No usar este producto con agua clorada”. |
| MYCOFLOR 200 mg/ml SOLUCIÓN PARA ADMINISTRACIÓN EN AGUA DE BEBIDA PARA PORCINO (3405 ESP) |
En el apartado 4.5 de la Ficha Técnica, se incluye la siguiente frase: “No usar el medicamento con agua clorada”. En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluye información sobre síntomas neurológicos y muerte. |
| HISTODINE 10 mg/ml SOLUCIÓN INYECTABLE PARA BOVINO (3547 ESP) |
En el apartado 4.5 de Ficha Técnica y 12. del Prospecto, se incluye la frase: “Lavar inmediatamente las salpicaduras en la piel y los ojos”. |
| VECTRA 3D SOLUCIÓN SPOT-ON PARA PERROS (EU/2/13/156) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluye información sobre convulsiones. |
| PUREVAX RC LIOFILIZADO Y DISOLVENTE PARA SUSPENSIÓN INYECTABLE (EU/2/04/051/001) PUREVAX RCP LIOFILIZADO Y DISOLVENTE PARA SUSPENSIÓN INYECTABLE (EU/2/04/052/001) PUREVAX RCPCH LIOFILIZADO Y DISOLVENTE PARA SUSPENSIÓN INYECTABLE (EU/2/04/050/001) PUREVAX RCP FELV LIOFILIZADO Y DISOLVENTE PARA SUSPENSIÓN INYECTABLE (EU/2/04/048/001) PUREVAX RCPCH FELV LIOFILIZADO Y DISOLVENTE PARA SUSPENSIÓN INYECTABLE (EU/2/04/047/001) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto se incluye información sobre vómitos. |
| NIFENCOL 100 mg/ml SOLUCION PARA ADMINISTRACION ORAL PARA PORCINO (3055 ESP) |
En el apartado 4.9 de la Ficha Técnica, se incluye la frase “No usar este producto con agua clorada”. |
| CEPHACARE SABOR 1000 mg COMPRIMIDOS PARA PERROS (3519 ESP) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluye información sobre síntomas digestivos. |
| FELIMINTIC 80/20 mg COMPRIMIDOS PARA GATOS (3573 ESP) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluye información sobre síntomas neurológicos. |
| DRONTAL PLUS COMPRIMIDOS CON AROMA PARA PERROS GRANDES (3587 ESP) |
En el apartado 4.4 de Ficha Técnica, se incluyen advertencias sobre la reinfección en perros. En el apartado 4.5 de Ficha Técnica, se incluye información sobre la ingestión accidental. En el apartado 4.6 de la Ficha técnica, se incluyen los signos de hiperactividad y diarrea. |
| FLUNISHOT 50 mg/ml SOLUCIÓN INYECTABLE PARA BOVINO, CABALLOS Y PORCINO (3833 ESP) |
En el apartado 4.5 de Ficha Técnica y 12 del Prospecto, así como en el apartado 5.2, se incluye información sobre toxicidad en aves necrófagas y precauciones para evitar la entrada del principio activo en la cadena alimentaria de la fauna salvaje. |
| NOBIVAC DHP (3192 ESP) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluye información sobre reacciones anafilácticas. |
| FRONTLINE SPOT ON GATO (1163 ESP) |
En el apartado 4.4 de Ficha Técnica, se incluye información sobre la necesidad de tratarse a todos los animales de la casa para un control óptimo. |
| BIOESTROVET 0,250 mg/ml SOLUCIÓN INYECTABLE PARA BOVINO (3518 ESP) |
En el apartado 4.5 de Ficha Técnica, se incluyen advertencias sobre el contacto directo con piel y mucosas, mujeres embarazadas y precauciones de uso. En el apartado 4.7, se incluye la advertencia sobre el uso del producto en lactación a criterio veterinario. En el apartado 4.10 se incluye información sobre los síntomas tras la sobredosificación y la no existencia de antídotos. |
| HIPRABOVIS IBR MARKER LIVE LIOFILIZADO Y DISOLVENTE PARA SUSPENSIÓN INYECTABLE PARA BOVINO (EU/2/10/114/001) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluye información sobre reacciones de hipersensibilidad y anafilaxia. |
| SUPRELORIN 9,4 mg IMPLANTE PARA PERROS SUPRELORIN 4,7 mg IMPLANTE PARA PERROS (EU/2/07/072/001-003) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluye información sobre convulsiones epilépticas (muy raras) tras la administración. |
| CYDECTIN POUR-ON AL 0,5% P/V PARA GANADO VACUNO (1140 ESP) |
En el apartado 4.3 de Ficha Técnica, se actualiza la información añadiendo la contraindicación en otras especies. En el apartado 4.5 de Ficha Técnica, se actualiza la información. En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluye información sobre signos neurológicos. |
| ALAMYCIN L.A 300 (1319 ESP) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluye información sobre anafilaxias. |
| INHIBACTEN L.A. 200 mg/ml (2531 ESP) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluye información sobre anafilaxias. |
| OXITEVALL 200 mg/ml L.A. (2649 ESP) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluye información sobre anafilaxias. |
| TENALINA L.A (980 ESP) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluye información sobre anafilaxias. |
| TERRALON 200 mg/ml L.A. (2739 ESP) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluye información sobre anafilaxias. |
| TERRAMICINA 100 mg/ml L.A. (2299 ESP) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluye información sobre anafilaxias. |
| TERRAMICINA 200 mg/ml L.A. (2161 ESP) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluye información sobre anafilaxias. |
| DOXYCARE 40 mg COMPRIMIDOS PARA GATOS Y PERROS (3846 ESP) |
En el apartado 4.3 de Ficha Técnica, se incluye información sobre la contraindicación en animales con insuficiencias renal o hepática o fotosensibilización conocida, o en cachorros. En el apartado 4.5 de Ficha Técnica, se incluye información sobre la administración. En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluye información sobre signos digestivos y dentales. En el apartado 4.10 de Ficha Técnica, se incluye información sobre los efectos de la sobredosificación de 5 veces la dosis recomendada. |
| DOXYCARE 200 mg COMPRIMIDOS PARA GATOS Y PERROS (3847 ESP) |
En el apartado 4.3 de Ficha Técnica, se incluye información sobre la contraindicación en animales con insuficiencias renal o hepática o fotosensibilización conocida, o en cachorros. En el apartado 4.5 de Ficha Técnica, se incluye información sobre la administración. En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluye información sobre signos digestivos y dentales. En el apartado 4.10 de Ficha Técnica, se incluye información sobre los efectos de la sobredosificación de 5 veces la dosis recomendada. |
| PAROFOR 140 mg/ml SOLUCIÓN PARA ADMINISTRACIÓN EN AGUA DE BEBIDA, LECHE O LACTORREMPLAZANTE (3569 ESP) |
En el apartado 4.4 de Ficha Técnica, se incluye información sobre resistencias cruzadas con algunos antimicrobianos. En el apartado 4.5 de Ficha Técnica y 12 del prospecto, se incluyen recomendaciones para el uso. |
| NEPTRA GOTAS ÓTICAS EN SOLUCIÓN PARA PERROS (EU/2/19/246/001) |
En el apartado 4.6 de Ficha Técnica y 6. del Prospecto, se incluyen efectos adversos en oído en el caso de perros de edad avanzada. |
Hay que tener en cuenta que algunos de los dictámenes iniciales acordados pueden sufrir alguna modificación durante el procedimiento administrativo de implementación, ya que los titulares disponen de un plazo para realizar las alegaciones que estimen conveniente. Del estudio de estas alegaciones, pueden derivarse cambios en las modificaciones inicialmente acordadas por el CSMV, que son las que finalmente se introducen en la ficha técnica, prospecto y, en su caso, en el etiquetado. El resto de modificaciones de la autorización de comercialización (por adaptación de los textos al nuevo QRD, un total de 37 productos) fueron tratadas en este Comité únicamente para información de sus miembros.
Comité Técnico del Sistema Español de Farmacovigilancia de Medicamentos Veterinarios (CTSEF-VET)
El CTSEF-VET es el órgano colegiado de la AEMPS encargado de unificar los criterios de funcionamiento y evaluar las señales de MV detectadas por el Sistema Español de Farmacovigilancia de Medicamentos Veterinarios (SEF-VET).
Es importante destacar que cuenta con la participación de todas las comunidades autónomas y de las ciudades autónomas de Ceuta y Melilla.
Se celebró una reunión en 2022, conjuntamente con el CSMV, donde cabe destacar la revisión de las actividades de los distintos agentes en base a las obligaciones recogidas en el documento de buenas prácticas de farmacovigilancia veterinaria, del Sistema Español de Farmacovigilancia Veterinaria. Además, se discutieron los informes preparados por el DMV relativos a los procedimientos de detección de señales realizados a nivel europeo y nacional.
Asimismo, se revisaron las estadísticas nacionales de farmacovigilancia veterinaria; se analizaron las novedades referentes a farmacovigilancia veterinaria que introduce el Reglamento (UE) 2019/6 del Parlamento Europeo y del Consejo; las alertas de farmacovigilancia, y la situación específica de algunos medicamentos a nivel nacional.
Alertas e informaciones de seguridad no urgente (NUIS) por razones de farmacovigilancia
En el 2022 no se decretó ninguna alerta por razones de farmacovigilancia.
En el 2022 recibieron y gestionaron, por afectar a MV registrados en España, seis NUIS.
Alertas por defectos de calidad
En el 2022 se decretó una alerta por defectos de calidad:
Promoción de la farmacovigilancia veterinaria
La promoción de la farmacovigilancia sigue siendo un punto estratégico para la AEMPS, además de una obligación legal contemplada en las directivas europeas, en el Real Decreto 1246/2008 y en el Real Decreto 1157/2021 que derogó al del 2008. Esta prioridad se fundamenta en que la UE considera crucial incrementar los niveles de notificación, por lo que se ha incluido este objetivo en la planificación estratégica del Grupo de Jefes de Agencias de la UE (HMA) y en su Subgrupo de Estrategias de Farmacovigilancia (ESS).
En 2022 se impartieron charlas técnicas destinadas a la formación de futuros veterinarios en las facultades de Veterinaria de: Barcelona, Cáceres, Córdoba, Madrid (Universidad Alfonso X y Universidad Complutense), Lérida, Murcia, Las Palmas de Gran Canaria, Valencia (Universidad Católica de Valencia y Universidad Cardenal Herrera Oria), León y Zaragoza, así como charlas a colegios veterinarios, como el de Salamanca.
Del mismo modo se participó en el Master de Farmacoepidemiología y Farmacovigilancia, organizado por la Universidad de Alcalá de Henares, y en el Máster de Sanidad Animal de la Fundación Vet+i.
Participación en reuniones internacionales
En relación con las actividades de FV a nivel europeo en 2022, cabe destacar la participación en los siguientes grupos y comités: Grupo de Farmacovigilancia Veterinaria del CVMP, P-SMEG, Subgrupo de Terminología VEDDRA, Subgrupo Quality Data y Subgrupo ESS de HMA.

