Esta web está dirigida a los responsables de vigilancia de productos sanitarios de los centros sanitarios y se ha elaborado de forma conjunta con las comunidades autónomas en el seno del Comité Técnico de Inspección de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS).
- Reglamentación de los productos sanitarios
- ¿En qué consiste el sistema de vigilancia de productos sanitarios?
- Designación de la figura del responsable de vigilancia de productos sanitarios
- Funciones y responsabilidades del responsable de vigilancia de productos sanitarios
-
Procedimiento para notificar los incidentes graves con productos sanitarios
- ¿Qué significa incidente e incidente grave?
- ¿Cómo se comunican los incidentes graves?
- ¿Cuál es el papel del responsable de vigilancia en la comunicación de incidentes graves?
- ¿Qué sucede con las comunicaciones de incidentes graves recibidas?
- Acceso al producto que se sospecha que está implicado en el incidente grave
-
Alertas de productos sanitarios
- Alertas de vigilancia de productos sanitarios
- Alertas de control de mercado de productos sanitarios
- ¿Qué se entiende por notas informativas de la AEMPS?
- Difusión de alertas de productos sanitarios y notas informativas por las autoridades sanitarias
- ¿Qué difusión debe hacer el centro de las alertas y notas informativas y qué papel desempeña el responsable de vigilancia en la difusión y en la aplicación de las actuaciones establecidas en las mismas?
-
Tarjetas de implante y registros nacionales de implantes
- ¿Qué información se debe aportar en la tarjeta de implante?
- ¿Qué productos deben ir acompañados de una tarjeta de implante?
- ¿Qué obligaciones tienen los centros sanitarios respecto a las tarjetas de implante?
- Registros nacionales de implantes
- ¿Cuál es el papel del responsable de vigilancia respecto a la información de los productos sanitarios implantables?
1. Reglamentación de los productos sanitarios
Este documento está dirigido a los responsables de vigilancia de productos sanitarios de los centros sanitarios y se ha elaborado de forma conjunta con las comunidades autónomas en el seno del Comité Técnico de Inspección de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS).
Los productos sanitarios y los productos sanitarios de diagnóstico in vitro (en adelante, en el término “productos sanitarios” se entenderá que también están incluidos los productos sanitarios de diagnóstico in vitro) están regulados a nivel europeo por los siguientes reglamentos:
Reglamento 2017/745 del Parlamento y del Consejo, de 5 de abril de 2017, sobre los productos sanitarios.
Reglamento 2017/746 del Parlamento y del Consejo, de 5 de abril de 2017, sobre los productos sanitarios para diagnostico in vitro.
Asimismo, en España están regulados por los siguientes reales decretos:
Real Decreto 192/2023, de 21 de marzo, por el que se regulan los productos sanitarios.
Real Decreto 942/2025, de 21 de octubre, por el que se regulan los productos sanitarios de diagnóstico in vitro.
Estos reales decretos establecen los requisitos nacionales aplicables a la notificación de incidentes graves por parte de los profesionales sanitarios y la designación de un responsable de vigilancia por los centros sanitarios.
Dicha normativa está disponible en la página web de la AEMPS.
El Anexo I de este documento incluye información general de interés sobre los productos sanitarios.
-
Notificación de incidentes graves
Si un profesional sanitario tuviera conocimiento de un incidente grave que pudiera estar relacionado con un producto sanitario, debe notificarlo a la AEMPS. Para llevar a cabo esta notificación, se ha habilitado en la página Web de la AEMPS la plataforma de notificación, NotificaPS.
-
Designación del responsable de vigilancia
Para establecer los procedimientos necesarios para asegurar el cumplimiento de los requisitos legislativos relativos a la vigilancia de los productos sanitarios por parte de los profesionales sanitarios, los centros sanitarios deben disponer de la figura del responsable de vigilancia.
El responsable de vigilancia debe supervisar los procedimientos relativos a la vigilancia de productos sanitarios en su centro como, por ejemplo, la notificación de incidentes graves de los que tuvieran conocimiento los profesionales sanitarios o la implementación de las acciones correctivas de seguridad relacionadas con productos sanitarios de las que haya sido informado por el fabricante. Por otra parte, también es responsable de supervisar que se cumple con las obligaciones establecidas en la regulación europea respecto a las tarjetas de implante y la información relevante aportada por el fabricante que acompañan a algunos productos implantables.
2. ¿En qué consiste el sistema de vigilancia de productos sanitarios?
El sistema de vigilancia de productos sanitarios engloba la notificación de incidentes graves ocurridos con productos sanitarios, su registro y evaluación, la adopción de medidas oportunas para la protección de la salud y la transmisión de estas medidas a los agentes interesados.
Su objetivo es mejorar la protección de la salud y la seguridad evitando la repetición de incidentes graves, mediante la recogida, evaluación y difusión de la información sobre los citados incidentes y la adopción de las medidas correctivas apropiadas.
Toda la información relacionada con las directrices para la aplicación del sistema de vigilancia por los centros y profesionales sanitarios se está disponible en la página web de la AEMPS.
3. Designación de la figura del responsable de vigilancia de productos sanitarios
Los centros sanitarios que deberán designar expresamente un responsable de vigilancia son los siguientes:
- Centros sanitarios con internamiento (hospitales).
- Centros especializados sin internamiento:
- Centros de cirugía mayor ambulatoria.
En el resto de los centros sanitarios, la responsabilidad de vigilancia de los productos sanitarios recaerá en el director médico o el responsable sanitario del centro que conste en el Registro de Centros y Servicios Sanitarios de la comunidad autónoma correspondiente.
Los profesionales idóneos para ser designados como responsables de vigilancia cuentan con titulación universitaria sanitaria, ejercen un puesto de responsabilidad en el centro, dentro de servicios/unidades horizontales que puedan asumir la coordinación de la recepción y transmisión de información a los servicios especializados tales como: directores médicos, jefes de servicio/sección de farmacia, medicina preventiva, calidad, seguridad del paciente, enfermería, entre otros.
Se debe cumplimentar el “Formulario de comunicación de la designación del responsable de vigilancia de productos sanitarios a las autoridades sanitarias” que se puede encontrar en el anexo II.
El formulario debe estar firmado por el representante legal del centro sanitario y por el responsable de vigilancia designado. Los centros sanitarios remitirán este formulario completado y firmado a las autoridades sanitarias de la correspondiente comunidad autónoma y a la AEMPS. Los centros sanitarios pertenecientes a la Red Sanitaria de la Defensa efectuarán dicha comunicación a través de la Inspección General de Sanidad de la Defensa, quien la trasladará a la AEMPS y a las autoridades sanitarias de la correspondiente comunidad autónoma.
En caso de cambio de responsable de vigilancia el centro deberá cumplimentar un nuevo formulario con los datos del nuevo responsable designado e, igualmente, comunicar a las autoridades sanitarias de la correspondiente Comunidad Autónoma y a la AEMPS o a la Inspección General de Sanidad de la Defensa, en su caso.
El Directorio de los puntos de vigilancia de productos sanitarios de las comunidades autónomas para la comunicación de la designación del responsable de vigilancia se puede encontrar la web de la AEMPS.
4. Funciones y responsabilidades del responsable de vigilancia de productos sanitarios
El responsable de vigilancia tiene las siguientes funciones:
Supervisar, en su centro, el cumplimiento de las obligaciones establecidas en el artículo 35 del Real Decreto 192/2023, de 21 de marzo, por el que se regulan los productos sanitarios y del artículo 30 del Real Decreto 942/2025, de 21 de octubre, por el que se regulan los productos sanitarios para diagnóstico in vitro, relacionadas con el sistema de vigilancia.
Supervisar y coordinar el cumplimiento, por parte de los profesionales sanitarios del centro, del procedimiento establecido de notificación a las autoridades sanitarias de incidentes graves o potencialmente graves asociados con la utilización de productos sanitarios, de los que tenga conocimiento en el ejercicio de su actividad sanitaria.
Actuar como interlocutor del centro con las autoridades sanitarias, en materia de vigilancia de productos sanitarios.
Facilitar a las autoridades sanitarias la documentación que le sea requerida para la investigación de los incidentes graves notificados.
Garantizar la difusión, a los profesionales sanitarios implicados de su centro, de las notas informativas/alertas de productos sanitarios emitidas por la AEMPS y transmitidas por las autoridades sanitarias autonómicas competentes, y supervisar, en su caso, la aplicación de las medidas establecidas en la misma.
Velar por el cumplimiento de las obligaciones establecidas en el artículo 36 del Real Decreto 192/2023, de 21 de marzo, por el que se regulan los productos sanitarios, en relación con las tarjetas de implante.
5. Procedimiento para notificar los incidentes graves con productos sanitarios
Un incidente con un producto sanitario incluye todo funcionamiento defectuoso o deterioro de las características o el funcionamiento de un producto comercializado, incluidos los errores de uso debidos a características ergonómicas del producto, así como cualquier inadecuación de la información facilitada por el fabricante o cualquier efecto colateral indeseable.
Un incidente con un producto sanitario de diagnóstico in vitro es todo funcionamiento defectuoso o deterioro de las características o el funcionamiento de un producto comercializado, incluidos los errores de uso debidos a características ergonómicas, así como cualquier inadecuación de la información facilitada por el fabricante y cualquier daño como consecuencia de la decisión médica o la acción emprendida u omitida sobre la base de la información o los resultados proporcionados por el producto.
La notificación de incidentes por parte de los profesionales sanitarios es obligatoria en el caso de incidentes graves.
Un incidente grave es todo incidente que, directa o indirectamente, haya podido tener o haya tenido alguna de las siguientes consecuencias:
El fallecimiento de un paciente, usuario u otra persona
El deterioro grave, temporal o permanente, de la salud de un paciente, usuario u otra persona
Una grave amenaza para la salud pública
Algunos ejemplos de un deterioro grave, temporal o permanente, de la salud de un paciente, usuario u otra persona, son:
Enfermedad o lesión con amenaza para la vida.
Deterioro permanente de una función corporal o daño permanente de una estructura corporal.
Proceso que necesita una intervención médica o quirúrgica para evitar un deterioro permanente de una función corporal o un daño permanente de una estructura corporal. Por ejemplo: Un aumento clínicamente significativo de la duración de un procedimiento quirúrgico, una condición que precise hospitalización o suponga prolongar notablemente la misma.
Un incidente grave que suponga una grave amenaza para la salud pública sería aquel que pudiera tener como resultado un riesgo inminente de muerte, deterioro grave de la salud de una persona o enfermedad grave que pueda requerir una actuación correctiva rápida y que pueda causar morbilidad o mortalidad significativa en los seres humanos, o que sea poco frecuente o imprevisto en relación con el lugar y el momento de que se trate.
Algunos ejemplos de amenazas serias para la salud pública pueden ser:
Enfermedades contagiosas, como el virus de la inmunodeficiencia humana (VIH), la enfermedad de Creutzfdt-Jakob (ECJ), el ébola, el virus Zika, el síndrome respiratorio agudo grave (SARS).
Alto riesgo de padecer una enfermedad (por ejemplo, cáncer) como consecuencia de que el paciente haya estado expuesto al uso de un producto sanitario que afecta a una parte importante de la población o a un grupo específico de pacientes (por ejemplo, personas diabéticas o pacientes con problemas cardiacos) o a población vulnerable como niños, ancianos o mujeres embarazadas.
Exposición a componentes tóxicos que tienen un efecto potencialmente perjudicial para las personas.
Ataque cibernético relacionado con productos de soporte vital.
Conforme a la definición de incidente grave, es importante resaltar que los profesionales sanitarios y centros también deben notifica los incidentes graves que potencialmente podían haber tenido lugar. Es decir, también deben notificar aquellos casos en los que un fallo en el funcionamiento del producto podría haber dado lugar a la muerte o a un deterioro grave del estado de la salud o a una grave amenaza de salud pública pero que, debido bien a circunstancias afortunadas o a la intervención del personal sanitario, no ha llegado a producirse. Por tanto, no ha llegado a ocurrir un incidente grave pero potencialmente, en otras circunstancias, el fallo del producto sí hubiera podido ocasionar graves daños y esta situación debe ser notificada igual que otros incidentes graves.
En el Anexo III a este documento podrá encontrar una relación de ejemplos de incidentes por categorías de productos que se deben comunicar.
La AEMPS ha desarrollado el portal NotificaPS destinado a la notificación de incidentes graves relacionados con productos sanitarios por profesionales de la salud, usuarios y pacientes. La implementación de este portal facilita la notificación de incidentes graves por parte de los profesionales sanitarios y habilita una vía directa de notificación para los usuarios y pacientes.
Este portal permite la cumplimentación de toda la información relativa al incidente grave notificado, en función del producto involucrado, así como la posibilidad de adjuntar documentación adicional relevante: imágenes, historia clínica, pruebas diagnósticas, etc.
De esta manera, los profesionales sanitarios notificarán los incidentes graves de los que tengan conocimiento al portal NotificaPS puesto a disposición en la página web de la AEMPS.
Al entrar en el portal NotificaPS encontrará la siguiente pantalla:
Una vez dentro el profesional sanitario deberá cumplimentar el formulario con los datos necesarios para la investigación del incidente. Aunque solo hay algunos campos obligatorios, es recomendable aportar la mayor información posible para facilitar la investigación.
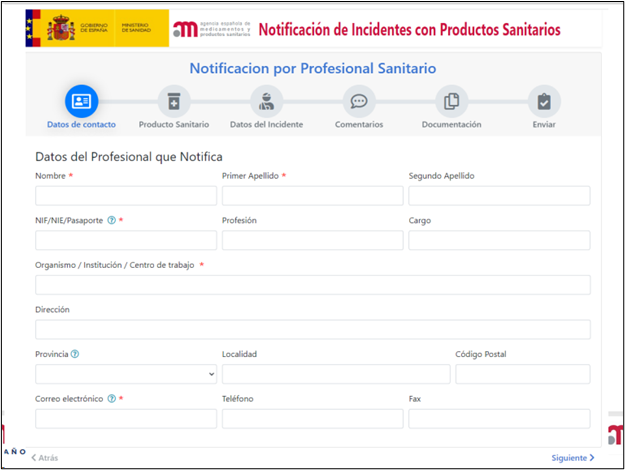
Supervisión, coordinación, facilitación y fomento de las notificaciones de incidentes en el centro
El responsable de vigilancia de productos sanitarios debe supervisar y coordinar el cumplimiento, por parte de los profesionales sanitarios del centro, del procedimiento establecido de notificación a las autoridades sanitarias de incidentes graves asociados con la utilización de productos sanitarios de los que tenga conocimiento en el ejercicio de su actividad sanitaria. Es decir, debe asegurarse de que los profesionales sanitarios de su centro notifican los incidentes graves detectados a las autoridades sanitarias y que la notificación se efectúa de acuerdo con el procedimiento establecido en el documento de Directrices para la aplicación del sistema de vigilancia por los centros y profesionales sanitarios.
Con el fin de facilitar el cumplimiento de dicha obligación, se debería elaborar, en el centro, un procedimiento normalizado de trabajo de gestión y notificación de incidentes graves de productos sanitarios que recogiese el procedimiento descrito en la página web de la AEMPS, de tal manera que el responsable de vigilancia siempre tenga conocimiento de los incidentes que se producen en su centro.
Asimismo, el responsable de vigilancia debería fomentar la notificación de incidentes graves por parte de los profesionales sanitarios.
Interlocutor con las autoridades sanitarias
Además, el responsable debe actuar como interlocutor del centro con las autoridades sanitarias, en materia de vigilancia de productos sanitarios, facilitando a éstas la documentación e información que le sea requerida para la investigación de los incidentes graves notificados por su centro, tanto por parte de las comunidades autónomas (CCAA) como de la AEMPS.
Registro de incidentes graves notificados
Por último, el responsable de vigilancia debería llevar un registro documentado de los incidentes graves asociados a productos sanitarios detectados en su centro sanitario, y notificados a las autoridades sanitarias.
Las notificaciones realizadas a través del portal de NotificaPS, se redirigirán al punto de contacto de vigilancia de productos sanitarios de su comunidad autónoma. Una vez enviada la comunicación, la persona que la haya realizado recibirá por correo electrónico un acuse de recibo con un localizador que permitirá consultar la información aportada.
Las comunidades autónomas validarán las notificaciones de incidentes graves recibidas, a través del portal NotificaPS, antes de su remisión al Área de Vigilancia de Productos Sanitarios de la AEMPS. Las notificaciones recibidas tras su revisión preliminar se registrarán en la base de datos de vigilancia de productos sanitarios. Una vez registrado el incidente grave, recibirán una referencia que le será remitida por correo electrónico junto con el localizador recibido al inicio.
Para la remisión de cualquier información adicional relacionada con la notificación, deberá hacer mención a esta referencia y enviarla por correo electrónico a la dirección psvigilancia@aemps.es, añadiendo en copia al punto de contacto de vigilancia de su comunidad autónoma que podrá consultar en el Anexo V (Directorio de puntos de vigilancia de productos sanitarios).
La AEMPS remite la información recibida sobre los incidentes a los fabricantes del producto involucrado y les solicita que lleven a cabo una investigación y remitan los formularios oficiales con la información completa sobre el incidente y la investigación realizada. El fabricante, su representante autorizado en la Unión Europea o el distribuidor del producto puede ponerse en contacto con la persona que ha realizado la notificación con el fin de recabar la información necesaria para poder efectuar la investigación. La AEMPS podrá intervenir, en caso necesario, en la investigación del fabricante o iniciar una investigación independiente.
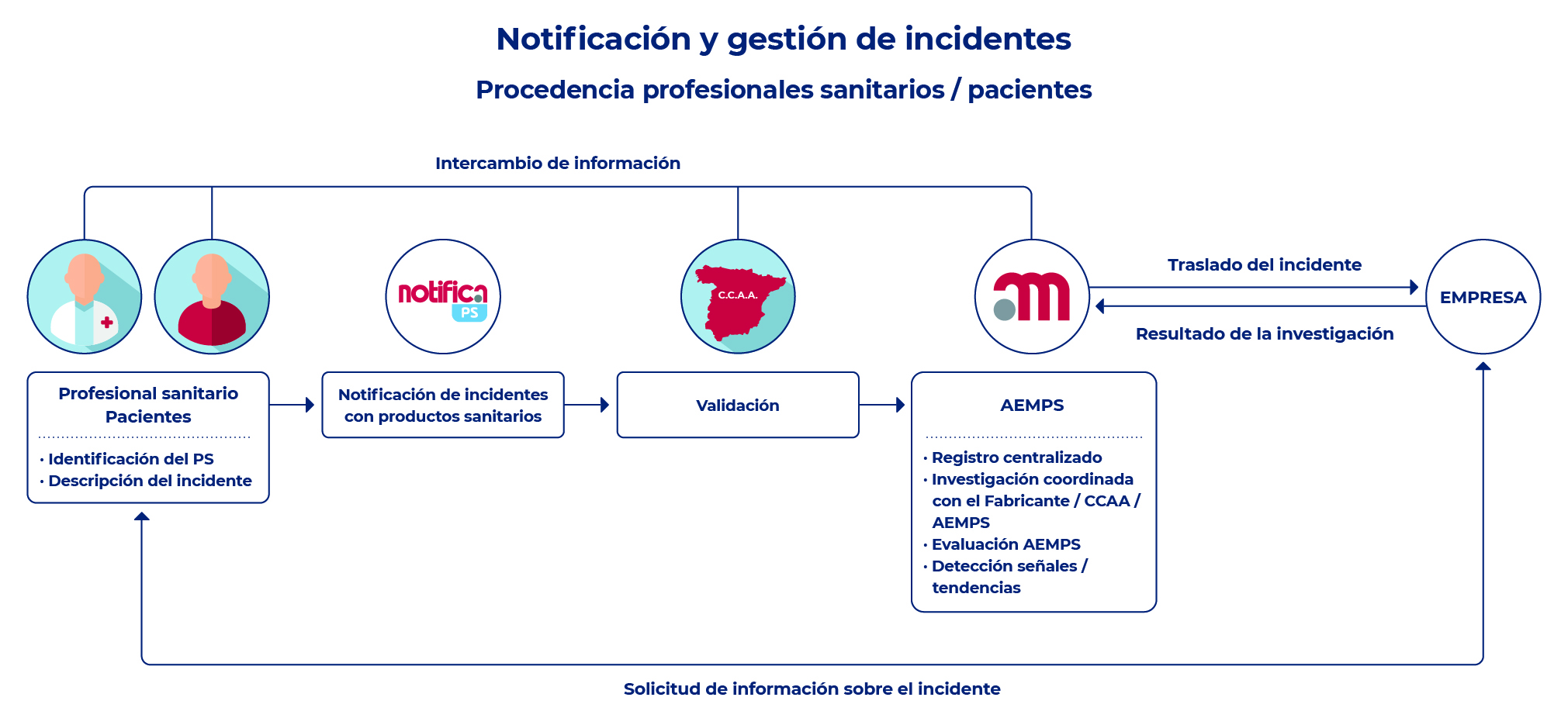
La notificación será considerada en el contexto de todas las demás notificaciones recibidas de los profesionales sanitarios y de los pacientes, por lo que de forma general no se emitirá un informe final individualizado por cada caso. No obstante, la AEMPS registra los incidentes graves notificados con el fin de identificar cualquier problema o defecto relacionado con los productos sanitarios. Este registro posibilita la asociación de casos y la generación de indicios de fallos de productos, así como la valoración de la repercusión de los hechos y en caso necesario, la adopción de las medidas correctoras pertinentes.
Los reglamentos europeos exigen que el registro y la evaluación de los incidentes graves se realice de forma centralizada y que las medidas que se adopten, junto con los hechos que han dado lugar a estas medidas, se comuniquen a la Comisión Europea y al resto de los Estados miembros.
En España, la AEMPS, es el organismo competente para la recepción y el registro de las notificaciones de incidentes graves y acciones correctivas de seguridad de productos sanitarios que se producen en España. La AEMPS es igualmente el punto nacional de la red de vigilancia europea de productos sanitarios y del International Medical Device Regulators Forum (IMDRF, por sus siglas en inglés), a través de la cual se reciben y se transmiten los hechos y las medidas adoptadas a la Comisión Europea y al resto de estados miembros.
Entrega al fabricante
Los profesionales sanitarios y centros pueden entregar las muestras de los productos relacionados con los incidentes graves al fabricante o al distribuidor con el fin de que éste verifique la funcionalidad del producto y determine si ha habido alguna disfunción que pueda haber causado el incidente. Esto responde a que para comprobar el funcionamiento de los productos suele ser necesaria una serie de medios y tecnologías complejas que, por lo general, solamente están disponibles en las propias instalaciones de los fabricantes.
Los fabricantes están obligados a investigar todos los incidentes que se producen relacionados con sus productos y a comunicar a la AEMPS aquellos incidentes graves ocurridos en nuestro país, que hayan producido la muerte o un grave deterioro en la salud o una grave amenaza para la salud pública, o bien que fueran de tal naturaleza que de producirse nuevamente pudieran provocar las mismas consecuencias.
Constancia de la entrega
Debe quedar constancia de la entrega del producto involucrado en el incidente grave al representante de la empresa, mediante la cumplimentación y firma del formulario del Anexo IV.
6. Alertas de productos sanitarios
Con carácter general, las alertas de vigilancia se generan tras la investigación de incidentes graves relacionados con un producto o tipo de productos, al detectarse problemas de funcionamiento o problemas por deficiencias en el etiquetado o en las instrucciones de utilización de los productos, que han causado o pueden causar un riesgo para la salud de los pacientes tratados con los mismos, o de los usuarios.
El objetivo de las alertas de vigilancia es poner en conocimiento de los profesionales y/o de los usuarios de dichos productos, los posibles riesgos y las medidas a adoptar para minimizarlos o eliminarlos.
6.1.1. Generación de acciones correctivas de seguridad por las empresas
-
¿Qué se entiende por Acción Correctiva de Seguridad (FSCA) y por Nota de Seguridad (FSN)?
Una Acción Correctiva de Seguridad (FSCA, por sus siglas en inglés) es una acción emprendida por un fabricante por motivos técnicos o médicos para evitar o reducir el riesgo de que ocurra un incidente grave relacionado con un producto comercializado. Tales acciones las notifica el fabricante por medio de una Nota de Seguridad.
Una Nota de Seguridad (FSN, por sus siglas en inglés) es, por tanto, una comunicación enviada por un fabricante a los usuarios o los clientes en relación con una acción correctiva de seguridad.
La FSCA puede incluir:
La devolución del producto sanitario al suministrador.
La modificación del producto.
El cambio de un producto por otro.
La destrucción del producto.
La adaptación del producto por el comprador según la modificación o cambio de diseño efectuado por el fabricante.
Las recomendaciones del fabricante en cuanto al uso del producto (por ejemplo, cuando un producto haya dejado de comercializarse o se haya retirado del mercado, pero podría estar todavía en uso, como es el caso de los implantes, o los cambios en la sensibilidad analítica o especificidad de los productos sanitarios para diagnóstico in vitro).
Actualización de las instrucciones de uso del producto.
Actualización del software.
-
¿Cuándo se genera una FSCA y una FSN?
De manera general, la FSCA suele iniciarla el propio fabricante/empresa comercializadora del producto que detecta el problema a través de los sistemas de garantía de calidad que tiene implementados en sus procesos de producción o control, o bien a través del seguimiento poscomercialización como es la recepción de reclamaciones o la notificación de incidentes, por parte, generalmente de los profesionales sanitarios que utilizan estos productos.
Cuando, como consecuencia de las investigaciones efectuadas y de la evaluación de los riesgos, el fabricante considera que existe un riesgo de muerte, de deterioro grave del estado de salud o de una grave amenaza de salud pública asociado al uso del producto, inicia una FSCA y la notifica a los clientes y/o usuarios mediante una FSN.
Por su parte la AEMPS, tras la valoración de la información, si es necesario, genera una alerta de vigilancia que transmite a los puntos de contacto de vigilancia de productos sanitarios de las comunidades autónomas (CCAA) tal y como se indica en el apartado 6.1.2.
-
¿Cuál es el papel del responsable de vigilancia en relación con las FSCA y FSN?
El responsable de vigilancia de productos sanitarios debe supervisar que el centro sanitario implementa adecuadamente las FSCA, tanto por parte de la empresa fabricante/comercializadora como por los profesionales sanitarios, en el ámbito de sus competencias.
Uno de los aspectos que debe supervisar, es si la empresa facilita la información y, en caso necesario imparte la formación que sea precisa para la correcta aplicación de las acciones correctivas de seguridad. También deberá asegurarse de que la información recibida llega a los profesionales que utilizan los productos afectados por la FSCA en su centro.
6.1.2. Generación de alertas de vigilancia por la AEMPS
Las situaciones que pueden dar lugar a que la AEMPS emita una alerta son las siguientes:
-
Como consecuencia de una FSCA emitida por un fabricante
La empresa notifica al Área de vigilancia de productos sanitarios de la AEMPS, así como a las autoridades sanitarias de todos los estados miembros afectados, mediante un formulario de FSCA, las medidas de seguridad que ha adoptado y la FSN que tiene previsto remitir a los centros afectados.
-
Como consecuencia de la recepción de reclamaciones o la notificación de incidentes por parte de:
Profesionales sanitarios/pacientes: la AEMPS recibe estas notificaciones a través del portal NotificaPS como se explica en el apartado 5.2.
Empresas: La empresa notifica al Área de Vigilancia de Productos Sanitarios de la AEMPS los incidentes graves que se producen en nuestro país, al igual que notifica al resto de estados miembros los incidentes graves que se producen en sus respectivos países y efectúa una investigación sobre los mismos.
-
Como consecuencia de alertas generadas por las autoridades sanitarias:
El Área de Vigilancia de Productos Sanitarios de la AEMPS, recibe igualmente alertas generadas por otras autoridades sanitarias tanto nacionales como de otros países.
El Área de vigilancia de productos sanitarios de la AEMPS evalúa las FSCA, las notificaciones de incidentes graves y las alertas recibidas de otras autoridades sanitarias, adoptando, en caso necesario, las medidas adicionales oportunas y transmitiéndola alerta a los puntos de contacto de vigilancia de productos sanitarios de las comunidades autónomas (CCAA) para la difusión a los centros de su ámbito territorial.
Se define «control del mercado» como las actividades llevadas a cabo y medidas tomadas por las autoridades públicas para controlar y garantizar que los productos cumplan los requisitos establecidos por la legislación de armonización de la Unión pertinente y no pongan en peligro la salud, la seguridad ni otros aspectos de la protección del interés público.
La Agencia es competente en la verificación de la conformidad de los productos sanitaros y en el control del mercado, que se realiza en colaboración con las autoridades sanitarias de las Comunidades Autónomas, así como junto con el resto de las autoridades europeas, velando por que los productos comercializados sean conformes con la legislación y tomando las medidas adecuadas para evitar su comercialización y uso por parte de los usuarios, en caso contrario. Este control de mercado está destinado a evitar que se ponga en peligro la salud, la seguridad y otros aspectos de la protección del interés público, lo que conlleva en ocasiones a la publicación de alertas de control del mercado.
Los incumplimientos de la legislación se detectan de forma proactiva a través de actividades planificadas por la AEMPS o a través de comunicaciones recibidas de las autoridades sanitarias, profesionales sanitarios, pacientes, empresas, asociaciones de usuarios, colegios profesionales, de fuerzas y cuerpos de seguridad del estado etc. Estas comunicaciones se realizan al área de control del mercado.
Entre los incumplimientos, se incluyen casos de defectos de calidad, problemas relacionados con el marcado CE, etc. También se incluyen los casos de productos sanitarios falsificados que son productos con una presentación falsa de su identidad o de su origen o de sus certificados de marcado CE o de los documentos relativos a los procedimientos de marcado CE, siempre que el incumplimiento se realice de manera voluntaria y con intencionalidad, entendiéndose sin perjuicio de las vulneraciones de los derechos de propiedad intelectual e industrial.
Los productos sanitarios falsificados se detectan generalmente por los propios fabricantes de los productos legalmente comercializados, mientras que los productos con marcados CE falsos y/o con certificados CE de conformidad falsos se suelen detectar a través de las autoridades sanitarias o los Organismos Notificados.
En estos casos tras la evaluación por el Área de Control del Mercado y en caso de que se detecte que existe un problema con un producto que se encuentra en el mercado y que pueda poner en riesgo la seguridad para los usuarios o pacientes, se ordenarán las medidas oportunas entre las que pueden estar: el cese de la comercialización del producto, retirada del producto del mercado, cese de utilización del producto, recuperación desde los usuarios así como establecimiento de medidas particulares de seguimiento por parte de los profesionales.
Estas medidas se comunicarán a través de una alerta de control de mercado que será transmitida por el AEMPS a los puntos de contacto de vigilancia de productos sanitarios de las comunidades autónomas para su difusión, si procede, en su ámbito territorial.
En ocasiones, la AEMPS transmite junto con la alerta una nota informativa en la que informa de los riesgos, las medidas adoptadas y recomendaciones para los agentes económicos, profesionales o para los pacientes o usuarios. Según la razón por la que se haya generado la nota informativa, ésta podrá ser:
Nota informativa relacionada con la seguridad en la utilización de los productos y/o en el seguimiento de los pacientes.
Nota informativa relacionada con los incumplimientos detectados en los productos sanitarios comercializados.
Estas notas se publican en la página web de la AEMPS.
El Área de Vigilancia de Productos Sanitarios de la AEMPS transmite a todas las CCAA las alertas y las notas informativas generadas.
En la transmisión de la alerta a los puntos de contacto de las CCAA, se envía la siguiente información:
La identificación, y finalidad del producto.
Descripción del problema identificado.
La nota de aviso con la información facilitada por el fabricante o distribuidor sobre el problema en el producto afectado, y las medidas que ha adoptado, en los casos en los que la alerta se genera como consecuencia de una FSCA.
La lista de distribución del producto o de los lotes o números de serie del producto sanitario afectado, en función de la información de distribución facilitada por el fabricante. Esta información es confidencial para la gestión de la alerta por las CCAA y no se difunde.
En las alertas de control del mercado, las no conformidades detectadas y las medidas ordenadas para los agentes económicos y/o profesionales sanitarios.
A partir del momento de la recepción de la alerta, los puntos de contacto de vigilancia de productos sanitarios de las CCAA activan sus procedimientos de actuación para la transmisión de la alerta a todos los centros afectados de su Comunidad Autónoma.
En los casos en los que el producto afectado no se haya distribuido en una Comunidad Autónoma, esta no difunde la alerta, salvo que se considere que debe difundirse de forma generalizada debido a la gravedad del caso y/o a la incertidumbre sobre el ámbito de distribución del producto.
En la siguiente figura se incluye un diagrama de flujo sobre la generación de alertas y notas informativas por la AEMPS y su difusión a los centros sanitarios por las autoridades sanitarias de las CCAA.
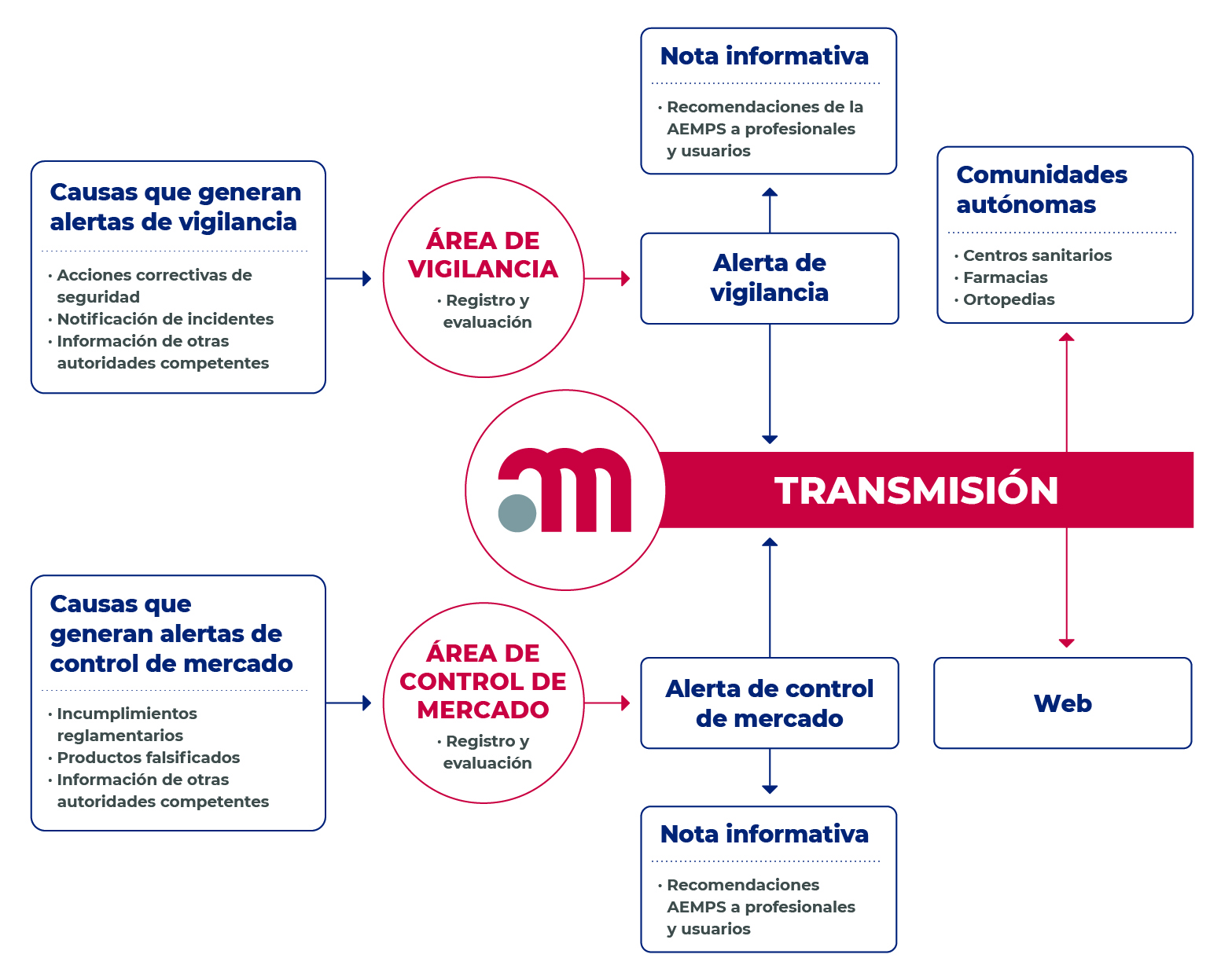
Los centros sanitarios deben disponer de un procedimiento normalizado de trabajo que describa el procedimiento de difusión de las alertas y notas informativas a los profesionales sanitarios implicados y defina las responsabilidades para su aplicación.
El responsable de vigilancia de productos sanitarios del centro debe:
Garantizar la difusión de las alertas y notas informativas de productos sanitarios emitidas por la AEMPS y transmitidas por las autoridades sanitarias autonómicas competentes, a todos los servicios/profesionales sanitarios de su centro que puedan estar afectados.
Supervisar, en su caso, la aplicación de las actuaciones establecidas en las alertas y notas informativas.
Mantener un registro de las alertas que haya recibido el centro y de la difusión que ha llevado a cabo de cada una de ellas en el que se consigne la fecha de transmisión a los servicios/profesionales sanitarios y el nombre de estos servicios/profesionales.
Además, el responsable de vigilancia de productos sanitarios, en los casos en que se requiera por la Comunidad Autónoma o por la AEMPS, deberá elaborar un informe de cierre de la alerta en el que se deben recoger los siguientes aspectos:
- Número de la alerta
- Fecha de la alerta
- Producto implicado
- Fabricante/distribuidor
- Motivo de la alerta
- Servicios/profesionales del centro a los que se ha difundido la alerta
- Acciones correctivas llevadas a cabo
- Acciones formativas impartidas
- Seguimiento de las acciones correctivas
- Fecha de cierre de la alerta
7. Tarjetas de implante y registros nacionales de implantes
Los fabricantes suministrarán junto con los productos sanitarios implantables y, al menos en castellano, una tarjeta de implante y otra información relevante.
En la tarjeta de implante, que tendrá el tamaño de una tarjeta de crédito, el fabricante debe incluir la siguiente información necesaria para la identificación del producto:
- Nombre del producto
- Tipo de producto
- Número de serie
- Número de lote
- Identificador único del producto (UDI)
- Modelo del producto
- Nombre, dirección y sitio web del fabricante
La información relevante que el fabricante proporcionará junto con la tarjeta de implante es la siguiente:
- las advertencias, precauciones o medidas que deba tomar el paciente o un profesional de la salud respecto de las interferencias recíprocas con influencias externas, exámenes médicos o condiciones ambientales razonablemente previsibles
- información sobre la vida útil prevista del producto y cualquier seguimiento necesario
- cualquier otra información que garantice una utilización segura del producto por parte del paciente, con inclusión de la información cualitativa y cuantitativa general sobre los materiales y las sustancias a las que pueden estar expuestos
El fabricante debe proporcionar la tarjeta de implante junto con la información relevante mencionada en el punto anterior con todos los productos sanitarios implantables excepto los siguientes:
- Material de sutura
- Grapas
- Materiales para obturación dental
- Aparatos de ortodoncia
- Coronas dentales
- Tornillos
- Cuñas
- Cables
- Placas
- Alfileres
- Clips
- Dispositivos de conexión
Los centros sanitarios deben de cumplimentar las tarjetas de implante para incluir la siguiente información:
Identificación del paciente
Nombre y dirección del centro sanitario o del profesional sanitario que realice la implantación del producto
Fecha de implantación
Los centros sanitarios entregarán al paciente la información relevante mencionada en el punto 7.1 junto con la tarjeta de implante cumplimentada. Toda esta información debe ser facilitada, al menos, en castellano.
El objetivo de proporcionar una tarjeta de implante a los pacientes es que:
Los pacientes puedan identificar el producto sanitario que tienen implantado para poder acceder a la información relativa al mismo.
Los pacientes puedan identificarse a sí mismos como portadores de los implantes y, por tanto, como pacientes que pueden necesitar una atención especial en determinadas situaciones.
El personal de urgencias u otras personas que atiendan al paciente puedan estar informados sobre las especiales necesidades o cuidados que requieren determinados pacientes en situaciones de urgencia.
Las comunidades autónomas podrán efectuar, en su caso, un requerimiento de la cumplimentación de las tarjetas por los centros sanitarios.
En el caso de que haya un Registro Nacional de Implantes, los centros y profesionales sanitarios tienen la obligación de comunicar a dichos registros los datos requeridos. Deben realizar estas sin perjuicio de la comunicación que, en su caso, sea exigida por las autoridades sanitarias de las comunidades autónomas donde se encuentren ubicados los centros sanitarios o los profesionales que los implanten.
El responsable de vigilancia de productos sanitarios debe velar por el cumplimiento de las obligaciones relacionadas con las tarjetas de implante, establecidas en el artículo 36 del Real Decreto 192/2023, de 21 de marzo, por el que se regulan los productos sanitarios.