Última actualización: 14/12/2016
Puede consultar esta nota en formato pdf Modificación de 14 de diciembre de 2016 (ver nota al final)* Modificación de 3 de junio de 2016 (ver nota al final)* Fecha de publicación: 27 de mayo de 2016 Categoría: INDUSTRIA, MEDICAMENTOS DE USO HUMANO Referencia: MUH, 7/2016
La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) ha adoptado una iniciativa para que, una vez que el Comité de Medicamentos de Uso Humano de la Agencia Europea de Medicamentos haya dictado Opinión Positiva para un medicamento centralizado, el Laboratorio Titular de la Autorización de Comercialización pueda con carácter voluntario presentar de forma telemática la «Solicitud de Código Nacional y del Material de Acondicionamiento para la Comercialización en España» a través de la aplicación informática de registro de medicamentos de uso humano RAEFAR II.
La AEMPS ha venido implantando una serie de mejoras con objeto de agilizar la tramitación de las autorizaciones y modificaciones de comercialización de medicamentos. Estas mejoras se quieren extender ahora también a los medicamentos que se tramitan por la Agencia Europea de Medicamentos a través del procedimiento centralizado, cuya autorización culmina con la preceptiva Decisión de la Comisión Europea, y que implica que la AEMPS asigne el código nacional para cada presentación, tras la revisión de una parte del material de acondicionamiento, y notifique todo ello tanto al TAC como a la Dirección General Cartera Básica de Servicios del SNS y Farmacia (DGCSF).
El TAC también se podrá acoger a este proceso de solicitud de registro en RAEFAR II con posterioridad a la Decisión de la Comisión, para cualquier otra presentación ya autorizada por la Agencia Europea de Medicamentos que pretenda comercializar.
En todo caso, para aquellos medicamentos en los que su titular decida no acogerse a esta iniciativa, la AEMPS seguirá realizando la carga en RAEFAR II. El titular podrá enviar la «Solicitud de Código Nacional y del Material de Acondicionamiento para la Comercialización en España» después de la Decisión de la Comisión, tal como se viene realizando hasta ahora, es decir, presentando la documentación por Registro General, pero en formato electrónico. A partir de ese momento la AEMPS procederá a revisar el material presentado y notificar la «Comunicación del Código Nacional» para la comercialización en España, y a la carga de las bases de datos.
En consecuencia, los titulares de medicamentos que se tramiten por procedimiento centralizado interesados en seguir la presente instrucción deberán ajustarse a lo siguiente:
-
AUTORIZACION INICIAL
-
Envío de la solicitud
Dictada la Decisión de la Comisión por la que se autoriza el medicamento, el titular podrá presentar telemáticamente la «Solicitud de Código Nacional y del Material de Acondicionamiento para la Comercialización en España» a través de RAEFAR II. Para proceder a dicha presentación, se debe realizar la correspondiente solicitud a través de la pestaña “Comunicación de Centralizados” disponible en Raefar II, indicando en los campos indicados de la solicitud, tanto el número de procedimiento global asignado por la EMA “EMA/CHMP/ XXXXXX/2016, como el del medicamento (EU/1/XX/XXX) y el/los formatos a comercializar (EU/1/XX/XXX/001-005). En la secuencia, se incluirá un formulario de solicitud eAF para Nuevas Autorizaciones de Medicamentos, por concentración o forma que pretenda comercializarse en España (asegúrese de utilizar la versión en vigor en el momento de la solicitud) disponible para su descarga en la web de Eudralex, o en esubmission, siendo imprescindible rellenar los apartados marcados como obligatorios para los productos centralizados, (en el caso de, por ejemplo, no estar disponible el código ATC, se indicaría el facilitado provisionalmente). Es altamente recomendado remitir UN solo eAF por forma farmacéutica y concentración, y poner las presentaciones asociadas a esa forma farmacéutica y concentración, que tengan intención de comercializar en España, en la sección 2.2. Los eAFs se incluirán en la carpeta m1/eu/form/es. Al envío de este formulario, se adjuntará la siguiente documentación:- Fotocopia, en español, de la Decisión de la Comisión por la que se autoriza el medicamento.
- Copia de la versión vigente de los Datos Administrativos Europeos (obtenida del expediente eCTD del dossier europeo de registros para este medicamento).
- eAF debidamente cumplimentado, bloqueado y guardado en formato digital.
- Textos en inglés y en español acordados tras la etapa de revisión de Comentarios Lingüísticos (Día 237 del procedimiento EMA Post-opinión)1.
- Propuesta de las maquetas del embalaje exterior para las presentaciones que se pretenden comercializar en España. El código nacional deberá aparecer como XXXXXX.X. En caso de que en el momento de esta presentación el laboratorio no conozca aún el número europeo de registro para cada presentación, éste se podrá indicar en la maqueta como EU/X/XX/XXX/XXX.
- Si procede, Certificado Braille correspondiente a dichas presentaciones.
- Dicha documentación se presentará en paralelo al envío del/ de las solicitudes en Raefar II, y se estructurará como una Secuencia NEES, incluyendo toda la documentación dentro del Módulo 1. Como anexo 1 a esta Instrucción se incluye un modelo de secuencia NEES para realizar dicho envío.
- Para cualquier duda sobre la carga en RAEFAR II se debe dirigir al correo electrónico “edossier@aemps.es”.
-
Notificación de la AEMPS
Si se ha seguido el proceso descrito, la AEMPS enviará en un plazo máximo de 7 días, a contar desde la presentación de la secuencia con la Decisión, y siempre que los materiales sean correctos, la Notificación de «Comunicación del Código Nacional para la comercialización en España». La AEMPS ha trabajado e implementado el desarrollo informático necesario para que se reciba dicha notificación por vía electrónica, mediante un mensaje de aviso a la dirección de correo electrónico que el solicitante indique en los apartados 2.4.1., 2.4.2. del/ de los formulario(s) eAF presentado/s (Titular, Persona designada por él). Dicha comunicación de resolución incluirá el código nacional asignado al formato para el que se solicitó. Al no haber punto para indicar Representante Local en los formularios de solicitud, este será indicado en la “cover” y será notificado también vía electrónica. Igualmente, la AEMPS ha desarrollado e implementado una comunicación automática y electrónica con la DGCSF, para que ésta reciba copia de dicha notificación de «Comunicación del Código Nacional para la Comercialización en España» en el mismo momento que se envía dicha comunicación electrónica al laboratorio. -
Comunicación de comercialización efectiva
De acuerdo con lo establecido en el artículo 28 del RD 1345/2007, el Laboratorio Titular debe comunicar de forma expresa a la AEMPS la fecha de comercialización efectiva de cada medicamento, como mínimo quince días antes de efectuarse dicha comercialización. Para señalar la fecha de comercialización efectiva se empleará la aplicación «Notificaciones sobre comercialización de medicamentos»2.
-
-
MODIFICACIONES DE AUTORIZACIÓN
-
Notificación de la modificación
Para aquellas modificaciones de los medicamentos centralizados que deban ser notificadas a la AEMPS, tal como se indica en el Anexo 2 de la presente instrucción, una vez obtenida la autorización de la autoridad competente, cuando proceda, el laboratorio utilizará la pestaña de RAEFAR II habilitada para enviar estas notificaciones (SOLICITUD/ MODIFICACIONES CENTRALIZADOS). En el Anexo 3 se muestra un ejemplo de la información a introducir por cada presentación, a la cual se adjuntará un envío de una Secuencia NEES que incluya la documentación pertinente en cada caso (Copia de la Decisión de la Comisión, textos nuevos, si procede, etc.). Para cualquier duda, se deberá dirigir al correo electrónico edossier@aemps.es. -
Transmisión de la información a la DGCSF
Una vez recibida esta comunicación por la AEMPS, ésta procesará la información, actualizará, si procede, la base de datos RAEFAR II, y enviará en su caso, de manera automática, una comunicación a la DGCSF, dando cuenta de este traslado, asimismo, al titular.
-
ANEXO 1. Modelo de secuencia NEES para realizar envío del formulario de RAEFAR
Ejemplo de un envío para 3 concentraciones o formas:
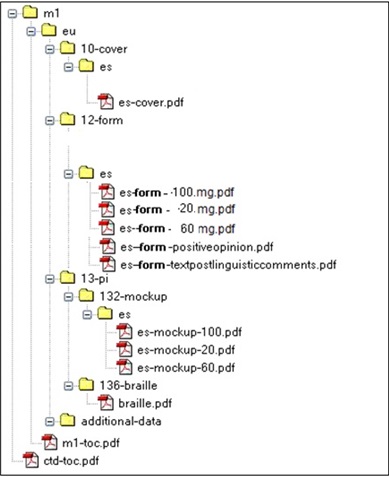
ANEXO 2. Relación de modificaciones que deben ser notificadas a la AEMPS para su traslado posterior a la DGCSF, si procede:
- Cambio del Titular o la dirección.
- Cambio de representante local o de la dirección.
- Cambio del nombre del medicamento.
- Cambio, supresión o nueva indicación terapéutica.
- Cambio o nueva posología.
- Cambio en las condiciones de prescripción.
- Cambio en el grupo terapéutico (ATC).
- Otros cambios relevantes en la ficha técnica (FT).
- Cambio de diseño del material de acondicionamiento.
- Comunicación de la anulación de un medicamento.
- Comunicación de la suspensión temporal de comercialización.
- Adición de nuevos formatos (nuevos C.N.) (No se requiere eAF).
ANEXO 3. Ejemplo de notificación de modificaciones de la autorización de comercialización de medicamentos autorizados por procedimiento centralizado en RAEFAR II
NOTA: Realizar un envío por presentación (EU/1/11/XXX/001). CAMPO DE TEXTO LIBRE A COMPLETAR EN RAEFAR: Producto y Breve descripción de la variación (por ejemplo: Nueva indicación, Cambio del Código ATC, Cambio de titular, Cambio del Representante local, etc.). Con fecha (día) de (mes) de (año) el laboratorio (Titular de la Autorización) ha recibido la Decisión de la Comisión para la modificación de (motivo de la modificación) para el/ los medicamento(s) (Nombre del medicamento). En España dicha modificación afecta a la(s) siguientes presentación(es) de dicho(s) medicamento(s):- Presentación 1 del Medicamento/ Nº de Registro Europeo/ C.N.
- Copia de la Decisión de la Comisión para dicha variación.
- Copia de la versión vigente de los Datos Administrativos Europeos (obtenida del expediente eCTD del dossier europeo de registros para este medicamento) (Si el cambio afecta a los datos administrativos – ej.: cambio de código ATC).
- Copia de la Información del Producto en español emitida con la Decisión de la Comisión (Anexos I-III) (Si el cambio afecta a dichos Anexos – por ej., cambio de indicación).
ANEXO 4. Instrucciones para los Titulares de la Autorización de Comercialización y Representantes Locales en lo relativo a los permisos de inclusión de datos de RAEFAR II
La inclusión de datos en RAEFAR II debe ser realizada por el Titular de la Autorización de Comercialización empleando medios propios o autorizando a un tercero. Puede encontrar la información detallada sobre cómo realizar esta solicitud en la web de la AEMPS, sección Sede Electronica.- Ver EMA/5542/02/Rev 4.1.: The linguistic review process of product info.
- https://sinaem.aemps.es/WebComercializacion/login.aspx?opc=humana
- https://sinaem.aemps.es/WebComercializacion/login.aspx?opc=humana

