Última actualización: 12/05/2016
Puede consultar esta información en formato pdf
Fecha de publicación: 12 de mayo de 2016
Categoría: PRODUCTOS SANITARIOS, CONTROL DEL MERCADO.
Referencia: PS, 6/2016
La AEMPS informa del cese de la utilización, cese de la comercialización y retirada del mercado de la solución oftálmica multidosis LUBRISTIL, fabricada por Farma Mediterrania, S.L., y distribuida por Angelini Farmacéutica, S.A., España, debido a defectos de calidad. No existen indicios de riesgo para la salud.
La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) ha sido informada por el Servicio de Control Farmacéutico y Productos Sanitarios de la Dirección General de Ordenación Profesional y Regulación Sanitaria del Departamento de Salud de la Generalitat de Cataluña, de las deficiencias de calidad detectadas en la fabricación de las soluciones oftálmicas fabricadas como producto sanitario por la empresa FARMA MEDITERRANIA, S.L., sita en C/ San Sebastià s/n, 08960 Sant Just Desvern, Barcelona, por lo que les ha requerido el cese de la fabricación y la retirada del mercado de los productos.
La empresa ANGELINI FARMACEUTICA, S.A., sita en C/ Osí 7, 08034 Barcelona, distribuye en nuestro país la solución oftálmica lubricante multidosis LUBRISTIL, fabricada por FARMA MEDITERRANIA, S.L. Este producto dispone de certificado de marcado CE emitido por el Organismo Notificado Noruego Det Norske Veritas Business Assurante, con número de identificación 0434.
Aunque no existen indicios de que los problemas detectados puedan suponer un riesgo para las personas que utilizan esta solución, la AEMPS, como medida de precaución, ha instado a la empresa ANGELINI FARMACEUTICA, S.A, a cesar la comercialización y retirar el producto del mercado.
La AEMPS no ha recibido notificaciones de incidentes adversos relacionados con este producto.
SITUACIÓN ACTUAL EN ESPAÑA
ANGELINI FARMACEUTICA, S.A, ha enviado una nota de aviso a las oficinas de farmacia y a los centros sanitarios, para advertir del problema detectado e informar de la retirada del producto.
IDENTIFICACIÓN DE LOS PRODUCTOS AFECTADOS EN ESPAÑA
- LUBRISTIL solución oftálmica lubricante MULTIDOSIS, envase muestra reducida 4 ml.
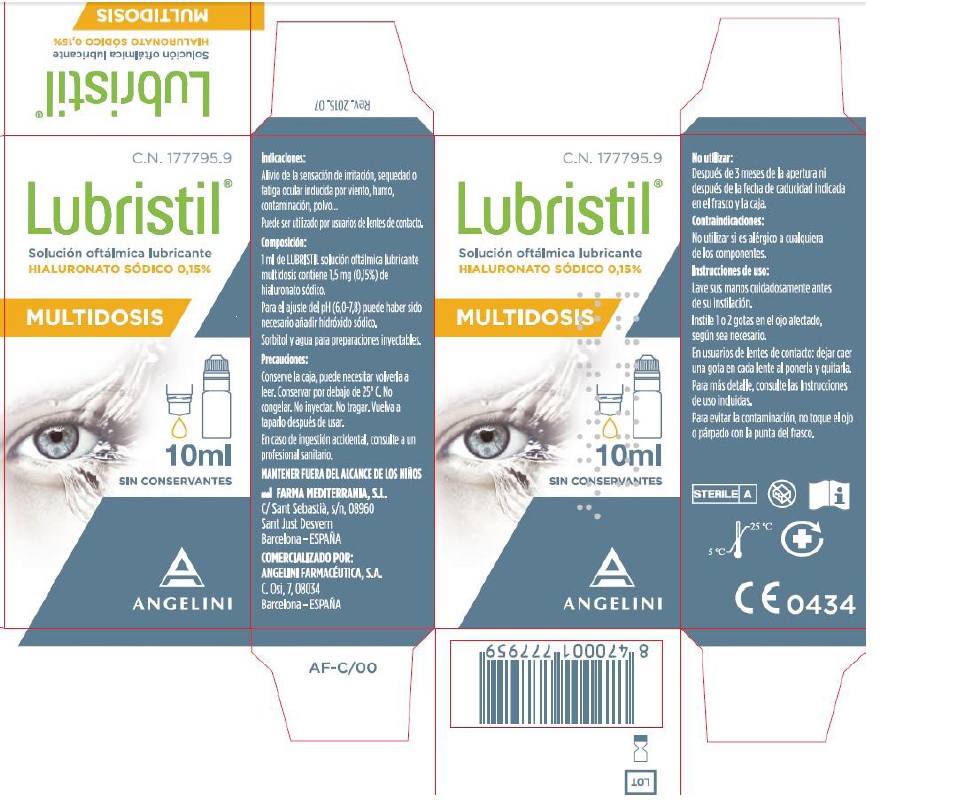
- LUBRISTIL solución oftálmica lubricante MULTIDOSIS, envase 10ml. (C.N. 177795.9)
-
RECOMENDACIONES
-
Pacientes
- Si usted dispone de la solución oftálmica lubricante multidosis LUBRISTIL, fabricada por FARMA MEDITERRANIA, S.L., distribuida por ANGELINI FARMACÉUTICA, S.A., y con el marcado CE acompañado del número 0434, deje de utilizarla y deséchela.
- Si usted dispone de otras soluciones oftálmicas LUBRISTIL, comercializadas por ANGELINI FARMACEÚTICA, S.A., pero de otro fabricante no le afecta esta comunicación y puede continuar utilizándolas.
-
Profesionales sanitarios de oficina de farmacia:
- Si dispone de la solución oftálmica lubricante multidosis LUBRISTIL (C.N. 177795.9) retírela de la venta y devuélvala a la empresa que se la suministró.
- Si ha vendido el producto citado anteriormente a pacientes, intente identificarlos y comparta con ellos esta información para que dejen de utilizarlo y lo desechen o le devuelvan el producto.
-
Profesionales sanitarios de centros sanitarios:
- Si dispone de la solución oftálmica lubricante multidosis LUBRISTIL envase muestra reducida 4 ml., no la entregue a pacientes y devuélvala a la empresa que se la suministró.
- Si ha entregado el producto de muestra a pacientes, comparta esta información con ellos para que lo dejen de utilizar y lo desechen.
Los profesionales sanitarios pueden comunicar cualquier incidente relacionado con el producto afectado, de acuerdo al procedimiento establecido en las Directrices para la aplicación del sistema de vigilancia por los centros y profesionales sanitarios (Ref.: AEMPS/CTI-PS/Octubre 2010) y los formularios relacionados.
DATOS DE LA EMPRESA
ANGELINI FARMACEUTICA, S.A.
C/ Osí 7.
08034 Barcelona.Teléfono: 932534505
Customerservice@angelini.es -
Pacientes

