La Comisión Europea (CE) estableció en 2014 un listado de sustancias activas que deben evaluarse de cara a su posible aprobación para su uso en los biocidas. Tras la evaluación de estas sustancias, la CE emite un reglamento de ejecución donde constan las sustancias que han sido aprobadas y sus condiciones específicas, o bien una decisión de ejecución donde se indican las sustancias que no han sido aprobadas.
En el caso de los biocidas competencia de la AEMPS, una vez que se aprueban las sustancias activas del producto biocida a nivel europeo, la autoridad competente para la autorización del producto, pasa a ser la Dirección General de Salud Pública y Equidad en Salud del Ministerio de Sanidad (DGSP). Actualmente los biocidas competencia de la AEMPS que están en revisión a nivel europeo conforme al programa de trabajo para el examen sistemático son:
- TP1: antisépticos para piel sana
- TP2: desinfectantes de ámbito clínico
- TP19: repelentes de uso humano
En el caso de productos con varias sustancias activas, pasarán a ser competencia de la DGSP una vez que se hayan aprobado todas las sustancias activas contenidas en dicho producto.
El reglamento europeo que marca todo este proceso ya prevé el cambio gradual y establece medidas transitorias, una serie de plazos a considerar tras la publicación del reglamento de aprobación de una sustancia activa o de la decisión de no aprobación.
A continuación, la Agencia ha desarrollado una descripción de las situaciones que pueden darse para los biocidas competencia de la AEMPS tras la evaluación europea de la sustancia activa.
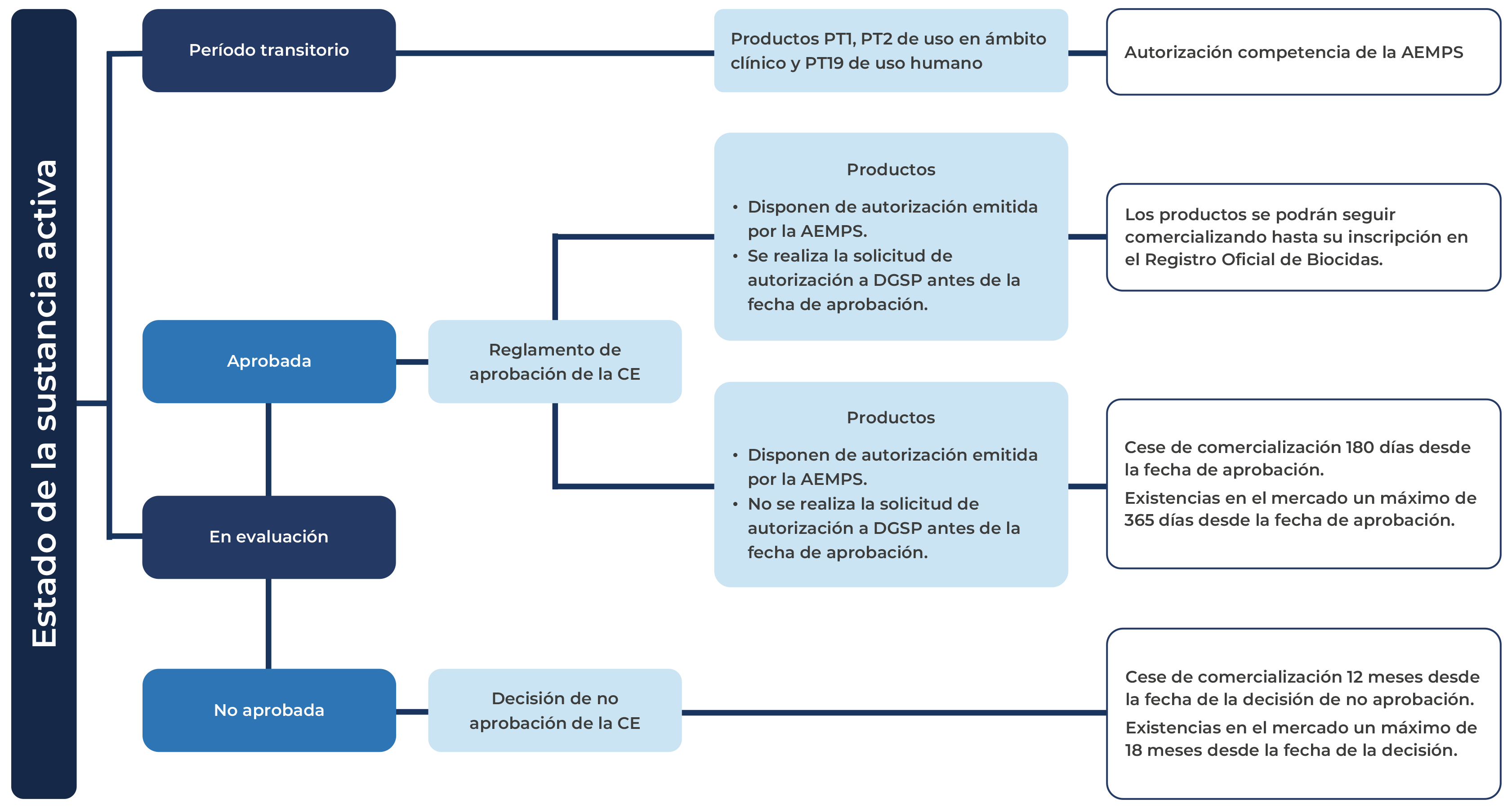
Publicación de un reglamento de aprobación de una sustancia activa
La AEMPS podrá emitir autorizaciones en base a la legislación nacional de aquellos biocidas de su competencia cuyas sustancias han sido evaluadas y aprobadas, hasta la fecha de aprobación de las sustancias. Estas autorizaciones tendrán una vigencia máxima de 3 años a partir de la fecha de aprobación de la sustancia activa.
En caso de productos con varias sustancias activas, estas autorizaciones en base a la legislación nacional se emitirán una vez que hayan sido aprobadas todas las sustancias activas contenidas en el producto.
Para biocidas competencia de la AEMPS cuyas sustancias activas han sido aprobadas, se admitirá la presentación de solicitudes de autorización hasta 6 meses antes de la fecha de aprobación de la última sustancia activa (para solicitudes nuevas, modificaciones y revalidaciones). Transcurrido ese plazo, no se admitirán nuevas solicitudes.
Para continuar en el mercado, los biocidas cuyas sustancias activas hayan sido aprobadas deben presentar un dossier para la autorización del producto conforme a la normativa europea ante la autoridad competente (en el caso de España la DGSP) antes de la fecha de aprobación de la última sustancia activa.
Tras la aprobación de una sustancia activa que dispone de una autorización emitida por la AEMPS pueden darse dos situaciones:
-
La empresa presenta una solicitud de autorización del producto a la DGSP antes de la fecha de aprobación.
Los productos se seguirán comercializando en periodo transitorio hasta su inscripción en el Registro Oficial de Biocidas. Los productos con comercialización permitida en periodo transitorio están listados en la página sobre productos biocidas y biosanitarios en periodo transitorio del Ministerio de Sanidad.
-
La empresa no presenta una solicitud de autorización del producto a la DGSP antes de la fecha de aprobación.
El biocida dejará de comercializarse a los 180 días de la fecha de aprobación de la sustancia o sustancias activas.
La utilización de las existencias del biocida podrá continuar hasta que hayan transcurrido un máximo de 365 días a partir de la fecha de aprobación de la sustancia o sustancias activas.
Publicación de una decisión de no aprobación de una sustancia activa
El biocida competencia de la AEMPS podrá seguir comercializándose durante un plazo máximo de doce meses a partir de la fecha de la decisión de no aprobación de la sustancia activa.
La utilización de las existencias que ya estén en el mercado del biocida podrá continuar hasta que haya transcurrido un plazo máximo de dieciocho meses a partir de la fecha de dicha decisión. El titular deberá comunicar a la AEMPS los últimos 5 lotes que se han puesto en el mercado.
- Reglamento (UE) nº 528/2012, del Parlamento Europeo y del Consejo de 22 de mayo de 2012 relativo a la comercialización y el uso de los biocidas.
- Reglamento Delegado (UE) nº 1062/2014 de la Comisión de 4 de agosto de 2014.
- Real Decreto 1054/2002, de 11 de octubre, por el que se regula el proceso de evaluación para el registro, autorización y comercialización de biocidas.

