Categoría: productos sanitarios, seguridad
Referencia: PS, 47/2024
- Estos apósitos para el cuidado de heridas pueden tener comprometida su esterilidad por un defecto en la bolsa del envase primario
- Se han detectado que en estas zonas de la bolsa del envase primario puede faltar polietileno o aparecer quemado o agrietado
- La Agencia establece una serie de recomendaciones de cómo actuar dirigidas a pacientes, profesionales sanitarios, distribuidores y farmacias
La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) ha tenido conocimiento, a través de Advanced Medical Solutions (AMS), Reino Unido, de un defecto en las bolsas del envase primario de determinados apósitos para el cuidado de heridas. En algunos lotes de estos apósitos se han detectado pequeñas zonas donde falta polietileno y zonas con polietileno quemado o agrietado en la cara interior del envase primario.
De acuerdo con la información facilitada por la empresa, estos defectos en la bolsa del envase primario del apósito podrían poner en peligro la esterilidad del producto. En el peor de los casos, podría dar lugar a una infección en el paciente.


Ejemplos de la quemadura de polietileno en la bolsa que contiene el apósito.
Situación actual en España
Los apósitos para el cuidado de heridas del fabricante Advanced Medical Solutions han sido distribuidos en España por Solventum (antes 3M) y Coloplast. Las empresas están enviando una nota de aviso dirigida a otros posibles distribuidores, farmacias, profesionales sanitarios y pacientes, para informarles del problema detectado y de las acciones a seguir.
Productos afectados
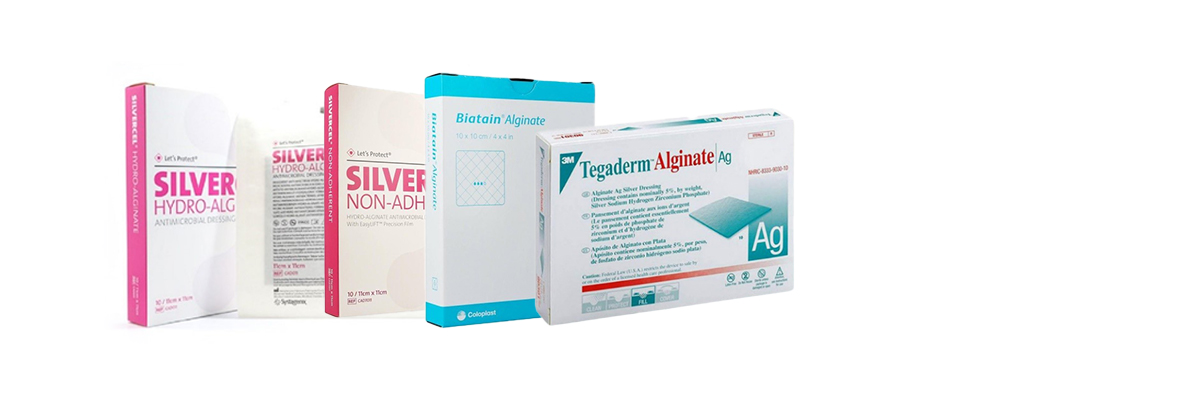
Los apósitos para el cuidado de heridas afectados de Advanced Medical Solutions (AMS), Reino Unido, son los siguientes. Las referencias y números de lote afectados se incluyen en la nota de aviso del fabricante:
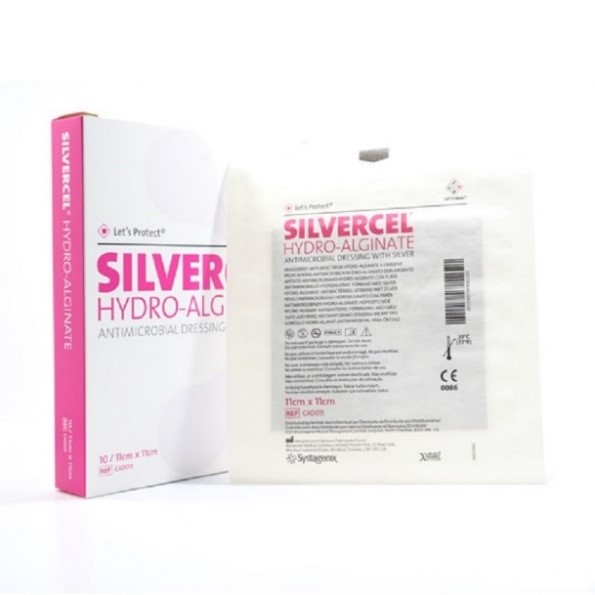
- Silvercel Hydro Alginate y Silvercel Non-Adherent
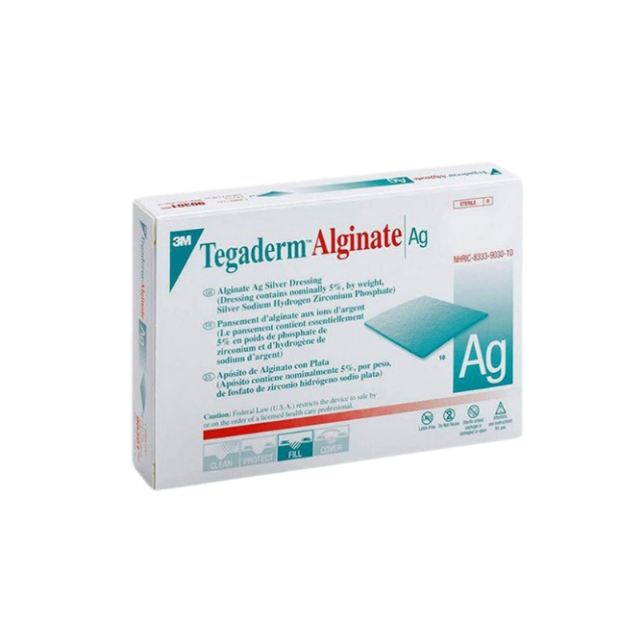
- Tegaderm Alginate
- ActivHeal Alginate, ActivHeal Aquafibre, ActivHeal Non-Adhesive Foam, ActivHeal Non Adhesive Tracheostomy, ActivHeal PHMB Foam Non-Adhesive, ActivHeal Raponicel Ultra
- Biatain Alginate
- Hyalo 4 High Gelling Fibre
- Calcicare Reinforced Alginate
- Reinforced Aquafibre
- Nurocel Extra
- Maxorb Extra


Información para pacientes
- Revise los apósitos que pueda tener en casa para identificar si alguno se corresponde con los indicados en el apartado de “Productos afectados”. Si es el caso, deje de utilizarlos.
- Si adquirió los apósitos en una farmacia, póngase en contacto con ella para que revisen si están afectados y le puedan proporcionar nuevos apósitos.
- Si los apósitos se los entregaron en su centro de salud, contacte con ellos o con el profesional sanitario que le realiza las curas, para que le proporcionen otros apósitos que no tengan este problema.
Información para profesionales sanitarios
- Inspeccione inmediatamente su inventario para identificar si tiene alguno de los apósitos indicados en el apartado de “Productos afectados”, e inspeccione la bolsa del envase primario en busca del defecto mencionado.
- En caso de tener alguno de estos apósitos afectados, no los utilice y póngalos en cuarentena a la espera de su destrucción segura.
- Siga las indicaciones de la nota de aviso de la empresa, remitiendo el formulario de respuesta y el certificado de destrucción de producto afectado.
- Si el producto se ha utilizado en algún paciente en un período de tiempo menor de tres meses, deberá vigilar a los pacientes para detectar posibles síntomas de infección por el uso de producto no estéril, durante el seguimiento clínico de rutina.
- Si tiene conocimiento de que algún paciente experimenta síntomas relacionados con esta nota de aviso, debe informar inmediatamente de ello a Advanced Medical Solutions y notificarlo a través del portal NotificaPS.
Información para farmacias
- Inspeccione inmediatamente su inventario interno en busca de alguno de los apósitos indicados en el apartado de “Productos afectados” para ver si presentan el defecto en el envase primario anteriormente mencionado.
- En caso de tener algún apósito con este defecto, póngalo en cuarentena a la espera de su destrucción segura.
- Siga las indicaciones de la nota de aviso de la empresa, remitiendo el formulario de respuesta y el certificado de destrucción de producto afectado.
Información para distribuidores
- Inspeccione inmediatamente su inventario en busca de alguno de los apósitos indicados en el apartado de “Productos afectados”, e inspeccione la bolsa del envase primario para ver si presenta el defecto del envase anteriormente mencionado.
- En caso de tener algún apósito con este defecto, póngalo en cuarentena a la espera de su destrucción segura.
- Siga las indicaciones de la nota de aviso de la empresa, remitiendo el formulario de respuesta y el certificado de destrucción de producto afectado.
- Distribuya inmediatamente esta nota de aviso a todos las personas usuarias finales/centros sanitarios afectados, e indíqueles que lleven a cabo las acciones descritas.
Datos de la empresa
Solventum (antes 3M ESPAÑA, S.L.)
Juan Ignacio Luca de Tena, 19-25,
28027 Madrid.
Coloplast Productos Médicos, S.A.
C/ Condesa de Venadito nº5 puerta 4,
28027 Madrid.
Si tiene conocimiento de algún incidente relacionado con el uso de un producto sanitario, notifíquelo a través del portal NotificaPS. Su colaboración notificando es esencial para tener un mayor conocimiento de estos productos y velar por su seguridad.