Categoría: productos sanitarios, seguridad
Referencia: PS, 10/2022
- La AEMPS ha sido informada de la sustracción de varias unidades del lote 2021120701 del “Test Antígenos rápido de saliva para Covid-19 HYGISUN”, fabricado por Anbio (Xiamen) Biotechnology Co., Ltd (China), e importado por Sunbeam International GmbH, Alemania
- En la investigación realizada por la AEMPS, se han identificado, además, otras unidades del test no conformes, que se están comercializando con el etiquetado e instrucciones de uso en alemán
- La Agencia establece una serie de recomendaciones de actuación dirigidas a distribuidores, oficinas de farmacia y personas usuarias
La empresa distribuidora Bolton Europe S.L, Madrid informó el 3 de febrero de 2022 a la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) de la sustracción en sus instalaciones de 12.900 unidades del lote 2021120701 del test de autodiagnóstico “HYGISUN Test Antígenos rápido de saliva para Covid-19”, fabricado por Anbio (Xiamen) Biotechnology Co., Ltd (China).
Según la información que figura en el etiquetado, el representante autorizado es la empresa Lotus B.V., Holanda, y el importador de esas unidades en Europa es la empresa Sunbeam International GmbH, Alemania.
En el caso de las unidades sustraídas, no se puede garantizar el adecuado mantenimiento de las condiciones de almacenamiento, conservación y distribución, lo que puede conllevar un riesgo por un fallo en el funcionamiento del test.
La AEMPS inició inmediatamente la consecuente investigación para conocer la distribución del lote 2021120701 y la situación del producto en el mercado español. Durante esta investigación, se han identificado además en el mercado otras unidades del test, que se están comercializando inadecuadamente con el etiquetado e instrucciones de uso en alemán, por lo que no cumplen los requisitos para comercializarse en nuestro país.
No obstante, es importante informar que hay unidades de este test del mismo fabricante que sí cumplen los requisitos de comercialización, ya que disponen del correspondiente marcado CE con los cuatro dígitos del organismo notificado y las instrucciones en castellano; teniendo asignado el Código Nacional 206191.0 (envase de 1 unidad) y código 206192.7 (envase de 5 unidades).
Situación actual en España
La AEMPS ha solicitado el cese de comercialización voluntario a los distribuidores identificados del “Test Antígenos rápido de saliva para Covid-19 HYGISUN”, fabricado por Anbio (Xiamen) Biotechnology Co., Ltd (China), importados por la empresa Sunbeam International GmbH, Alemania y que no cumplían con los requisitos de etiquetado e instrucciones en castellano.
Productos afectados
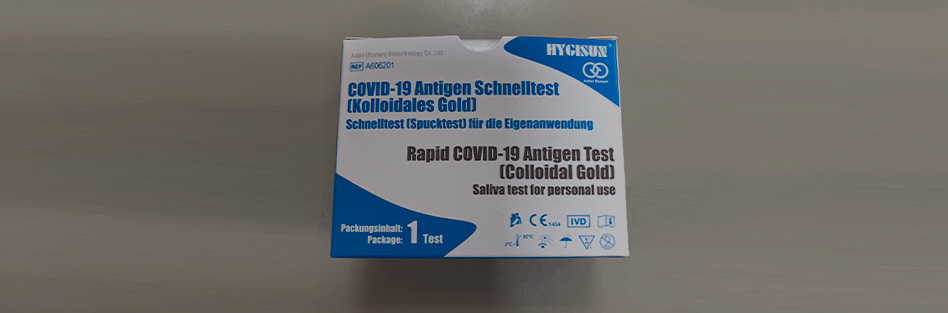
Los productos identificados como no conformes son aquellos en los que en su etiquetado aparece la marca “HYGISUN” y los datos del importador Sunbeam International GmbH, Alemania. Se incluyen fotografías del etiquetado para una mejor identificación.

Igualmente, se han detectado unidades de este producto no conformes, que han sido distribuidas con instrucciones de uso en el exterior de la caja y traducidas al castellano. Estas instrucciones no han sido revisadas o autorizadas por la AEMPS.
Información para distribuidores y oficinas de farmacia
- Examine sus registros de trazabilidad y compruebe si dispone de unidades del lote 2021120701 adquiridas a partir del 3 de febrero de 2022, o unidades del test con las instrucciones en otro idioma. En caso afirmativo, no las distribuya y retírelas de la venta. Compruebe el agente económico que se las ha distribuido con el fin de comprobar su legalidad.
- Únicamente se pueden comercializar productos que cumplan con los requisitos establecidos en la legislación cuando hayan sido debidamente suministrados, estén correctamente mantenidos y se utilicen conforme a su finalidad prevista, no comprometiendo la seguridad, ni la salud de los pacientes, personas usuarias ni, en su caso, terceros.
- Los productos sanitarios se deben adquirir a aquellos agentes que cuenten con la organización y medios precisos para garantizar que los productos sean conformes, y se garantice el adecuado almacenamiento y conservación de los mismos.
- Antes de comercializar un producto sanitario en España, se deben asegurar de que este posee el marcado CE y que va acompañado de los datos e informaciones específicas, tanto en etiquetado como en instrucciones, al menos en castellano.
- No obstante, de manera excepcional, la AEMPS ha permitido la comercialización de test de autodiagnóstico que carecían de etiquetado e instrucciones en castellano, siempre que se comercialicen con una traducción de estas al español, revisada por la Agencia y dirigida a las personas usuarias. Estos casos excepcionales están publicados en el siguiente enlace: https://www.aemps.gob.es/la-aemps/ultima-informacion-de-la-aemps-acerca-del-covid%E2%80%9119/informacion-general-sobre-tests-de-diagnostico-de-covid-19/#collapse501
- Si tiene conocimiento de un incidente relacionado con el uso de estos productos, notifíquelo al sistema de vigilancia de la AEMPS.
Información para la ciudadanía
- Adquiera únicamente los test de autodiagnóstico a través de las oficinas de farmacia. De esta manera, se garantiza el adecuado origen, almacenamiento y condiciones de conservación del test, y cuenta con la intervención de un farmacéutico con el asesoramiento correspondiente.
- Si tiene conocimiento de algún incidente relacionado con el uso de estos productos, notifíquelo a través del portal NotificaPS.